ボイルの法則(Mariotteの法則、Boyle–Mariotteの法則とも呼ばれる)は、理想気体に関する基本的な経験法則です。
この法則は次のように述べられます。
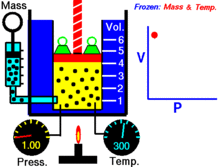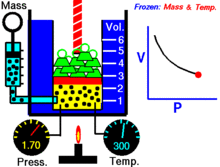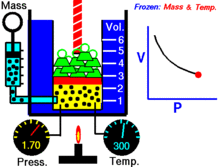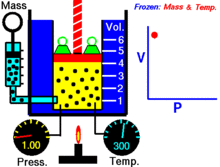
つまり、一定温度で一定質量の理想気体について、体積が小さくなると圧力は比例して大きくなり、その逆も成り立ちます。
P ∝ 1/V
または
PV = k
ここで、Pは気体の圧力、Vは気体の体積、kは一定(定数)です。体積が減少すると圧力が比例して増加し、その積PVは一定値kになります。
導出(理想気体の式から)
理想気体の状態方程式は次のように表されます。
PV = nRT
ここで n(モル数)と T(絶対温度)が一定であれば、右辺 nRT は一定値になり、したがって PV = const となります。これがボイルの法則です(等温過程における関係)。
変化前後の関係式
初めの状態の圧力を P1、体積を V1、変化後を P2、V2 とすると、どちらも同じ定数 k を持つため次が成り立ちます。
P1 V1 = k
P2 V2 = k
したがって、
P1V1 = P2V2
計算例(具体例)
例:あるガスの初期状態が P1 = 3 気圧、V1 = 5 L であるとします。圧力を P2 = 2 気圧に下げたときの体積 V2 を求めます。
P1V1 = P2V2
これを V2 について解くと:
V2 = (P1 V1)/P2
V2 = (3 × 5) / 2
V2 = 15 / 2
V2 = 7.5
したがって、圧力を 2 気圧に下げると体積は 7.5 L になります。
グラフと視覚的な特徴
P–V グラフ(横軸が体積 V、縦軸が圧力 P)では、ボイルの法則に従う等温過程は双曲線(反比例のグラフ)として表れます。曲線上の任意の点で PV の値は同じです。
単位と注意点
- 圧力の単位は Pa(パスカル)や atm(大気圧)など、体積は m³ や L(リットル)などを使います。計算時は必ず一貫した単位系に合わせてください(例:atm と L の組合せ、または Pa と m³ の組合せ)。
- ボイルの法則は「等温(温度一定)」かつ「一定量(モル数一定)の理想気体」に対して成立します。温度が変わる場合は PV = nRT を使います。
適用範囲と限界
実際の気体は高圧・低温の条件では分子間相互作用や分子の体積の影響が無視できなくなり、理想気体の仮定から外れます。こうした場合はボイルの法則からのずれが生じ、ファンデルワールス方程式など修正された状態方程式で扱います。
実験的検証・応用例
- 歴史的にボイルは J 字型管を用い、管内の気体と水銀で圧力と体積の関係を調べました(実験装置によって簡単に再現可能です)。
- 注射器や空気ポンプ、潜水艦のバラストタンク、水銀柱を用いた圧力計など、日常や産業で等温近似が成り立つ状況で応用されます。
- 等温過程で気体が外部に仕事をする量(仕事 W)は理想気体の場合 W = nRT ln(V2/V1) で表されます(温度一定のとき)。
この法則は1662年にロバート・ボイルによって最初に報告され、その後1679年にエドメ・マリオットによって独立に確認されました。現代では「ボイル–マリオットの法則」として知られています。