化学反応とは|定義・例・種類・反応速度・発熱・核反応との違い
化学反応の定義から身近な例、種類・反応速度、発熱の仕組み、核反応との違いまで図解と例でわかりやすく解説。
化学反応は、1つまたは複数の化学物質が1つまたは複数の他の化学物質に変化するときに起こります。例としては、以下のようなものがあります。
反応が速いものもあれば、遅いものもあります。また、温度などによって起こる速度が違うものもあります。例えば、木材は冷たいときは空気と反応しませんが、十分に高温にすると燃え始めます。エネルギーを出す反応もあります。これが発熱反応です。他の反応では、エネルギーを取り込んでしまう。これが発熱反応です。
核反応は化学反応ではありません。化学反応は原子の電子だけが関与しますが、核反応は原子核の中の陽子と中性子が関与します。
化学反応の基本的な説明(補足)
上の説明を補足します。化学反応では、原子同士の結合が切れたり新しくできたりして、出発物質(反応物)が別の物質(生成物)に変わります。反応中に原子そのものが消えることはなく、元素の種類と原子の総数は保存されます(質量保存の法則)。
代表的な例とその説明
- 鉄のさび:鉄(Fe)が酸素や水と反応して酸化鉄(さび)になる反応。上のリストの最初はこの例を示しています。
- 酢(酢酸)と重曹の反応:酢酸と炭酸水素ナトリウム(重曹)が反応して二酸化炭素を発生する中和反応+分解型の反応です(上のリスト参照)。
- 燃焼:有機物が酸素と反応して二酸化炭素や水、熱を出す反応(例:木材の燃焼)。
- 電気化学反応:電池の充放電や電気分解のように、電子の移動をともなう反応(上のリスト参照)。
反応速度(どれくらい速く進むか)
反応の速さは「反応速度」と呼ばれ、次のような要因で変わります。
- 濃度:反応物の濃度が高いほど分子同士の衝突頻度が増え、一般に速度は速くなります。
- 温度:温度が上がると分子の運動エネルギーが増え、衝突時に反応する確率が高くなるため、多くの場合速度が上がります(例として木材が高温で燃え始めること)。
- 触媒:触媒は反応の活性化エネルギーを下げて速度を上げますが、自身は反応前後で消費されません。
- 表面積:固体が関与する反応では、粉末状にすると表面積が増えて速度が上がります。
- 圧力:気体反応では圧力を上げると実効的な濃度が増し、速度が上がることがあります。
これらをまとめると、反応速度は「どれくらいの頻度で、かつどれだけの割合で反応物が生成物に変わるか」を示す量です。反応速度式やアレニウス則(温度依存性を表す式)を用いて定量的に扱います。
発熱反応と吸熱反応(エネルギーの出入り)
化学反応ではエネルギーの出入りがあります。外へエネルギー(主に熱)を放出する反応を発熱反応と呼びます(例:燃焼)。一方、周囲からエネルギーを取り込む反応を吸熱反応と呼びます。上の段落中に同じ表現が重複していましたが、実際には「エネルギーを出す=発熱反応」「エネルギーを取り込む=吸熱反応」が正しい区別です。
化学熱力学では反応の進行に伴うエンタルピー変化ΔHで表し、ΔHが負なら発熱、正なら吸熱です。また、反応には活性化エネルギー(反応を始めるためのエネルギー障壁)も存在し、触媒はこれを低くします。
化学反応の種類(代表)
- 合成反応(付加反応):二つ以上の物質が結合して一つの生成物になる反応(A + B → AB)。
- 分解反応:一つの物質が分かれて複数の生成物になる反応(AB → A + B)。
- 置換反応(単置換):ある元素や基が別のものと置き換わる反応。
- 二重置換(中和、沈殿):イオン交換によって新しい組み合わせができる反応(酸と塩基の中和、沈殿反応など)。
- 酸化還元反応(酸化・還元):電子のやり取りを伴う反応。電池や腐食、燃焼は典型例です。
- 酸・塩基反応:プロトンの授受を伴う反応。中和反応が代表的です。
- 触媒反応・酵素反応:触媒や酵素の存在下で進行する選択的で高速な反応。
核反応との違い(補足)
先に述べた通り、核反応は化学反応ではありません。化学反応は原子の外側にある電子の配置と結合の変化に基づく現象です。これに対して核反応は原子核の構成要素(陽子や中性子、場合によっては核力に関わる粒子)が変化し、質量欠損とそれに伴う莫大なエネルギー放出・吸収を伴います。核分裂・核融合・放射性崩壊などが核反応の例です。
実生活での関連事項と安全上の注意
- 日常生活では、さび・燃焼・調理時の化学変化・掃除(酸やアルカリの使用)・電池の充放電など、様々な化学反応が関わっています。
- 化学反応は有益な一方で、発熱や有毒ガスの発生、爆発の危険があるものもあります。化学薬品の取扱いや加熱、混合は安全データや手順に従って行ってください。
まとめ
化学反応は物質の結合が変わることで新しい物質ができる過程であり、速度やエネルギーの観点から様々な分類が可能です。反応の仕組み(電子の移動や結合の形成・切断)、速度に影響する因子、発熱・吸熱の区別、そして核反応との本質的な違いを理解することで、日常や産業での化学現象をより安全かつ効果的に扱えます。

たき火は酸化還元の例

錆びた鉄
基本的な4つのタイプ
合成
合成反応では、2つ以上の単純な物質が結合して、より複雑な物質を形成します。
A + B ⟶ A B {\displaystyle A+B\longrightarrow AB}.
"2つ以上の反応物が1つの生成物を与える"というのは、合成反応を識別するための別の方法です。合成反応の一例としては、鉄と硫黄を組み合わせて硫化鉄(II)を形成することが挙げられます。
8 F e + S 8 ⟶ 8 F e S {displaystyle 8Fe+S_{8}\longrightarrow 8FeS}.
他の例としては、単純な水素ガスと単純な酸素ガスを組み合わせて、水のようなより複雑な物質を生成することができる。
分解
分解反応とは、より複雑な物質がより単純な部分に分解されることです。したがって、合成反応とは逆の反応であり、次のように書くことができます。
A B ⟶ A + B {\displaystyle AB}
分解反応の一例としては、水を電気分解して酸素と水素ガスを作るものがあります。
2 H 2 O ⟶ 2 H 2 + O 2 {displaystyle 2H_{2}O\longrightarrow 2H_{2}+O_{2}}}} 2H_{2O
単一の取り替え
単一置換反応では、単一の未結合元素が化合物中の別の元素を置換することを意味します。言い換えれば、ある元素が化合物中の別の元素と場所を交換することです。
A + B C C ⟶ A C + B {\displaystyle A+BC\longrightarrow AC+B} A + B C + B {\displaystyle A+BC
一置換反応の一例としては、マグネシウムが水の中で水素に置き換わって水酸化マグネシウムと水素ガスになる場合がある。
M g + 2 H 2 O ⟶ M g ( O H ) 2 + H 2 {display style Mg+2H_{2}O\longrightarrow Mg(OH)_{2}+H_{2}}O
二重交換
二重置換反応では、2つの化合物のアニオンとカチオンが入れ替わり、2つの全く異なる化合物を形成します。これらの反応は、一般的な形式で行われます。
A B + C D ⟶ A D + C B {\displaystyle AB+CD\longrightarrow AD+CB} A B + C D ⟶ A D + C B {\displaystyle AB+CD\longrightarrow AD+CB
例えば、塩化バリウム(BaCl2)と硫酸マグネシウム(MgSO4)を反応させると、SO42-アニオンが2Cl-アニオンと入れ替わり、BaSO4とMgCl2という化合物が得られます。
二重置換反応の他の例としては、硝酸鉛(II)がヨウ化カリウムと反応してヨウ化鉛(II)と硝酸カリウムを生成する反応が挙げられる。
P b ( N O 3 ) 2 + 2 K I ⟶ P b I 2 + 2 K N O 3 {displaystyle Pb(NO_{3})_{2}+2KI\longrightarrow PbI_{2}+2KNO_{3}}}}}を表示します。
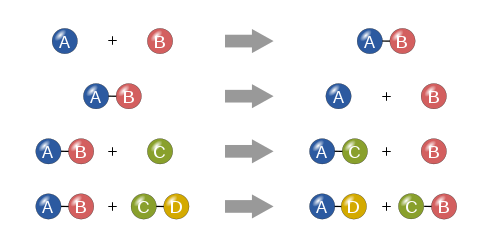
化学反応の基本となる4種類の反応:合成、分解、一重置換、二重置換
式
化学反応を式で表示しています。
A + B ⟶ C + D {\displaystyle 》 《A+B\longrightarrow C+D》}
ここで、AとBがCとDに化学反応を起こします。
燃焼反応の一例です。
C + O 2 ⟶ C O 2 {\displaystyle 》 《C+O_{2}\longrightarrow CO_{2}》}
関連ページ
- 有機反応
- レドックス
質問と回答
Q:化学反応とは何ですか?
A: 化学反応は、1つまたは複数の化学物質が1つまたは複数の他の化学物質に変化することで起こります。
Q: 化学反応の例を教えてください。
A: はい。化学反応の例としては、鉄と酸素が結合して錆を作る、酢と重曹が結合して酢酸ナトリウムを作る、二酸化炭素と水、物が燃えたり爆発したりする、光合成など生物の内部で起こる多くの反応が挙げられます。
Q: すべての化学反応は速いのですか?
A: いいえ、速い反応もあれば、遅い反応もあります。温度や他の要因によって、異なる速度で起こるものもあります。
Q: 発熱反応とは何ですか?
A: 発熱反応とは、エネルギーを放出する反応のことです。
Q: 吸熱反応とは何ですか?
A:吸熱反応とは、エネルギーを取り込む反応のことです。
Q: 核反応は化学反応に含まれますか?
A: いいえ、核反応は化学反応ではありません。化学反応には原子の電子だけが関与し、核反応には原子核の陽子と中性子が関与しています。
Q: 化学反応の速度に温度は影響しますか?
A: はい、温度や他のものによって、いくつかの反応は異なる速度で起こることがあります。例えば、木は冷たいと空気と反応しませんが、十分に熱くすると燃え始めます。
百科事典を検索する









