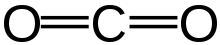二酸化炭素(CO2)は、化学物質の一種です。室温では気体で、無色・無臭・非可燃です。分子は1つの炭素原子と2つの酸素原子からなり、水に溶けて炭酸(薄い酸性)を作ります。人や動物は呼吸で二酸化炭素を放出し、息に含まれるCO2濃度は大気よりはるかに高くなります。また、有機物を燃やすと(火をつけると)、必ず二酸化炭素が発生します。植物は二酸化炭素を吸収して食物を作り、このプロセスは光合成と呼ばれます。二酸化炭素の性質は、1750年代にスコットランドの科学者ジョセフ・ブラックらによって初めて系統的に研究されました。
主な性質
- 物理的性質:無色・無臭の気体で、空気よりやや重い。常温常圧で気体、低温では固体(ドライアイス)になります。
- 化学的性質:還元性は弱く、単独では燃えませんが燃焼に伴って生成します。水に溶けると炭酸(H2CO3)を形成し、pHを下げます。
- 大気中濃度:産業革命前は約280 ppm(体積比)でしたが、化石燃料の燃焼などにより20世紀以降急増し、2020年代には約420 ppm前後に達しています。
発生源(どこから来るか)
二酸化炭素は自然起源と人為起源の両方があります。自然起源には、火山活動、土壌や森林の微生物による有機物分解、動植物の呼吸などがあります。人為起源では、石炭・石油・天然ガスなど化石燃料の燃焼、セメント製造などの産業プロセス、森林伐採による炭素放出が主要な原因です。日常生活では、車の排気、発電所、暖房、工場の排出などがCO2の主な供給源になります。
光合成と炭素循環
植物や藻類・シアノバクテリアは、大気中のCO2を取り込み、光エネルギーを使って有機物(グルコースなど)を合成します。簡略化した化学式は次のとおりです:
6 CO2 + 6 H2O → C6H12O6 + 6 O2。
このプロセスにより大気中の二酸化炭素は陸域・海洋の生物や土壌に一時的・長期的に固定され、地球規模の炭素循環を形成します。
温室効果と気候変動
二酸化炭素は温室効果ガスの一つであり、熱エネルギー(地表から放射される赤外線)を吸収・再放射することで大気中に熱を閉じ込めます。温室効果ガスは、私たちの惑星、地球の気候や天候を変化させる要因となり、これを一般に気候変動と呼びます。大気中CO2の増加は地表面の平均温度を上昇させる主要因で、結果として海面上昇、極端な気象の頻度増加、生態系や農業への影響などを引き起こします。こうした地球規模の気温上昇は地球温暖化と表現されます。
影響と安全性
- 低濃度(大気濃度レベル)では毒性はほとんどありませんが、閉鎖空間で高濃度になると酸素欠乏を招き、めまい・頭痛・意識喪失などを引き起こします。
- 人間の呼吸で排出されるCO2は室内換気の指標にもなり、室内のCO2濃度が上がると換気が必要です。
対策と削減方法
気候変動を抑えるためにCO2排出を減らすことが重要です。主な対策には以下があります:
- 化石燃料から再生可能エネルギーへの転換(太陽光、風力、地熱など)
- 省エネルギー・効率化(建物の断熱、電力使用の最適化、低燃費車の普及)
- 森林の保全・植林による自然の吸収源の強化
- 技術的手法としての炭素回収・貯留(CCS)や直接空気回収(DAC)
- 消費者レベルでのライフスタイル変化(肉の消費抑制、公共交通の利用など)
二酸化炭素は本来、地球にとって重要な成分ですが、その濃度を急激に増やすことは気候や生態系、社会に大きな影響を与えます。持続可能な社会を目指すためには、個人・企業・国際社会が連携して排出削減と適応策を進めることが求められます。