炭素(元素C)とは|性質・同素体・用途をわかりやすく解説
炭素(元素C)の性質・同素体(ダイヤモンド、グラファイト、フラーレン)と日常・産業での用途を図解と例でわかりやすく解説。初心者向け入門ガイド。
炭素は、化学記号Cの非常に重要な化学元素であり、地球上のすべての既知の生物は炭素を必要としている。炭素は原子量12、原子番号6。非金属であり、金属ではないことを意味する。
鉄は炭素と合金になると、硬い鋼鉄になる。石炭に含まれる炭素は重要な燃料である。
炭素の基本的な性質
- 原子番号と質量:原子番号は6で、主要な同位体であるC-12の質量数は12です。自然界の炭素はC-12とC-13(安定同位体)が主で、放射性同位体のC-14は年代測定に使われます。
- 電子配置と結合性:炭素は価電子を4つ持ち、4本の共有結合を作れるため多様な構造(鎖、環、網目)を形成します。これが有機化合物の基盤です。
- 非金属性:金属のように光沢や延性は持ちませんが、多様な物理的性質(極めて硬いものからやわらかいものまで)を示します。
同素体(同じ元素だが構造が違うもの)
炭素は同素体が多く、それぞれ性質が大きく異なります。代表的なもの:
- ダイヤモンド:3次元の網目状結晶で非常に硬く、光をよく屈折させるため宝石や切削工具に利用されます。
- 黒鉛(グラファイト):層状構造で層間が弱いため滑りやすく、鉛筆の芯や潤滑剤、電極材料として使われます。電気を良く通します。
- フラーレン・フラーレン類:分子状の球状や楕円状の構造を持ち、ナノテクノロジーや材料研究で注目されています。
- グラフェン:単原子層のシートで非常に高い電気伝導性と強度を持ち、電子材料や複合材料の研究対象です。
- カーボンナノチューブ:巻き上げたグラフェンの筒状構造で、強度や導電性に優れます。
- 無定形炭素(石炭、コークス、活性炭など):結晶性が低く、吸着材や燃料、精錬用の還元剤として使われます。
用途と応用例
- エネルギー源:石炭や石油などの化石燃料は主に炭素化合物から成り、燃焼して熱や電力を生みます。
- 金属の強化:鉄に炭素を加えると鋼(鉄鋼)になり、建築・機械・工具など広範な用途があります(上記の例を参照)。
- 有機化学と材料:プラスチック、薬品、染料などあらゆる有機化合物は炭素を骨格に持ちます。カーボンファイバーは高強度・軽量材料として航空・自動車・スポーツ用品に使われます。
- 電極・導電材料:黒鉛やグラフェンは電極・センサー・エレクトロニクスに利用されます。
- 環境・浄化:活性炭は吸着による浄水・空気清浄に有効です。
- 年代測定:放射性同位体C-14は考古学や地質学で年代測定(放射性炭素年代測定)に使われます。
- ナノテクノロジー:カーボンナノチューブやフラーレン、グラフェンは次世代の電子材料や複合材料として期待されています。
生物と地球環境における役割
- 生命の基礎元素:炭素はタンパク質、脂質、炭水化物、核酸など生体分子の基本骨格であり、すべての既知の生命に不可欠です。
- 炭素循環:大気中の二酸化炭素(CO2)、海洋、土壌、有機物の間で炭素は循環します。生物・化学・地質学的プロセスが関与します。
- 気候変動との関連:人間活動による化石燃料の燃焼で大気中のCO2が増えると温室効果が強まり、地球温暖化の一因になります。
同位体と年代測定
- C-12:最も豊富な安定同位体(質量数12)。
- C-13:自然に存在する安定同位体で、化学分析(同位体比分析)に役立ちます。
- C-14:放射性同位体で、半減期は約5730年。有機物の年代測定に広く用いられます。
まとめと注意点
炭素は元素として極めて多様で、硬いダイヤモンドから柔らかい黒鉛、ナノ構造体まで多様な性質を示します。また有機化合物の基礎であり、生物や産業、環境に深く関わっています。一方で化石燃料の燃焼によるCO2排出は気候変動問題と直結するため、利用と管理には注意が必要です。
炭素の化学
化学の一種である有機化学は、炭素とその化合物に関するものである。炭素は多くの種類の化合物をつくります。炭化水素は、炭素と水素を含む分子です。メタン、プロパン、その他多くの燃料は炭化水素です。人々が日常的に使っている物質の多くは、有機化合物です。
炭素、水素、窒素、酸素、そして硫黄やリンなどのいくつかの元素が一緒になって地球上のほとんどの生命を形成している(「生物学的に重要な元素のリスト」を参照)。炭素はそれ自身と他の元素とで強い結合を形成することができるので、非常に多くの有機化合物を形成しています。生物に含まれる炭素の量から、すべての有機物は「炭素系」とみなされる。各炭素原子は4つの単一共有結合を形成することができる。これらの結合により、炭素はプラスチックのようなポリマーと呼ばれる長い鎖状の分子を形成することができる。
語源
炭素の名前は、ラテン語で炭を意味するcarboに由来する。多くの外国語では、炭素、石炭、炭は同義語である。
カーボンの種類
自然界に存在する炭素は、ダイヤモンド、グラファイト、フラーレンという3つの同素体で存在する。黒鉛は粘土と一緒で、鉛筆に入っています。とても柔らかい。その中の炭素原子はリングを作り、それが重なり合ってとても滑りやすくなっています。ダイヤモンドは最も硬い天然鉱物です。フラーレンは、「サッカーボール」のような形をした炭素です。主に科学の分野で注目されている。カーボンナノチューブは、人工的に作られたチューブ状の炭素の同素体です。カーボンナノチューブは非常に硬いので、防具に使われるかもしれません。ナノチューブはナノテクノロジーに役立つかもしれません。
炭素の化合物は1,000万種類も知られている。
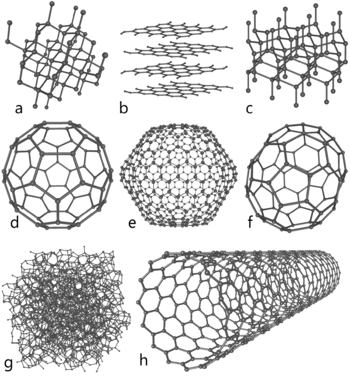
 a) ダイヤモンド、b) グラファイト、c) ロンズダライト、d-f) フラーレン(C60, C540, C70)、g) アモルファスカーボン、h) カーボンナノチューブ。
a) ダイヤモンド、b) グラファイト、c) ロンズダライト、d-f) フラーレン(C60, C540, C70)、g) アモルファスカーボン、h) カーボンナノチューブ。
放射性炭素年代測定法
炭素の放射性同位体である炭素14は、ある物体が何年前のものか、あるいは何かがいつ死んだのかを知るために使うことができる。地表にあるものが炭素を取り込んでいる間は、炭素14の量は変わりません。炭素を取り込まなくなると、炭素14の量は減ります。炭素14の半減期(放射性同位元素の半分がなくなるまでの時間)は5730年なので、炭素14がどれだけ残っているかで、その物体が何年前のものかを知ることができるのです。
ここで、カーボンは
炭素は宇宙のいろいろなところにある。古い星で最初に作られた。炭素は太陽の中で4番目に多い元素です。金星と火星の大気は、ほとんどが二酸化炭素です。
炭素は人体や他の生物にとって重要な元素であり、人体では全重量の23%を占め、2番目に多い元素である。また、多くの生体分子(生命に使われる分子)の重要な構成要素でもある。
地球上の炭素のほとんどは石炭である。黒鉛はスリランカ、マダガスカル、ロシアなど多くの(典型的な砂漠)地域にある。ダイヤモンドは希少で、主にアフリカで発見されている。炭素は一部の隕石にも含まれている。
質問と回答
Q:炭素の化学記号は何ですか?
A: 炭素の化学記号はCです。
Q:炭素の原子質量は?
A:炭素の原子質量は12です。
Q:炭素の原子番号は何番ですか?
A:炭素の原子番号は6です。
Q:炭素は金属か非金属か?
A:炭素は非金属であり、金属ではありません。
Q:鉄と炭素が合金になると、どうして硬い鉄になるのですか?
A:鉄と炭素が合金になると、硬い鉄になります。
Q:炭素を多く含む石炭から、どのような燃料を作ることができるのか?
A:炭素を多く含む石炭は、重要な燃料になります。

