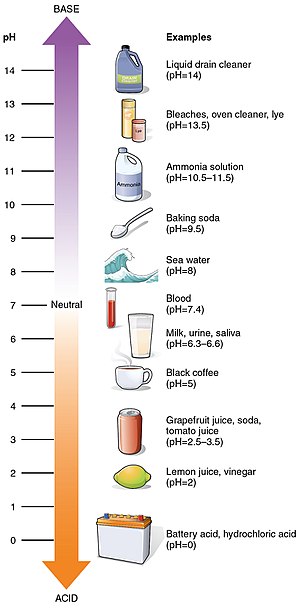
pHは溶液の酸性・アルカリ性を示す指標で、一般に0から14の尺度で表されます(ただし厳密には0–14に限定されるものではありません)。値が低いほど酸性、値が高いほどアルカリ性を示し、通常、酸性の溶液はpHが7未満、アルカリ性の溶液はpHが7より大きくなります。中性の溶液(例:純水)は、条件によりますが室温付近ではpH ≈ 7です。尺度としてのpHは、物質がどれだけ酸性かあるいはアルカリ性かを簡便に比較するために用いられます。
定義と起源
pHは溶液中の陽性の水素イオン(プロトン)の存在度合いを表す指標です。これは特に溶液中のプロトン(H+、実際にはヒドロニウムイオン H3O+ として存在することが多い)の「濃度」や「活性」を基に定義されます。化学者 S.P.L. ソーレンセンは1909年にpHの概念を導入しました。記号の由来は、pがドイツ語のpotenz(べき、指数、濃度を示す)を略したもの、Hは水素のイオン(イオンとしてのH+)を表しています。
計算式(濃度と活性)
教科書で最もよく示される式は、溶液中の水素イオン濃度 [H+](単位:モル/リットル)を用いた次の定義です。
pH = - log 10 [ H + ]
ここで [H+] は H+([H3O+] と表記されることもあります)の濃度を 1リットル当たりのモル数(モル度とも呼ばれる)で示したものです。例えば、[H+] = 1.0×10-7 mol·L-1 のとき pH = 7 になります(これは純水の代表値、25°C付近での例です)。
より正確には、pHは水素イオンの「活性」aH+を用いて定義されます。
pH = - log 10 [ a H + ]
活性 aH+ は理想希薄条件からの偏差(イオン間相互作用やイオン強度による効果)を考慮した値で、実務的には次のように書けます:
pHの範囲と極端な値
一般の水溶液ではpHは0から14付近に収まることが多いですが、極めて高い酸濃度や強塩基性条件では pH < 0 や pH > 14 となる場合があります。したがって pH を0–14に限定して考えるのは便宜的な近似であり、厳密には負の値や14を超える値もあり得ます。
pHと水の自動電離、pOH
水はわずかに自動電離しており、その平衡定数は温度に依存します。25°Cではイオン積 Kw = [H+][OH-] = 1.0×10-14 です。ここから
- pOH = -log10[OH-]
- pH + pOH = 14(25°Cの場合)
したがって、ある溶液の [OH-] が分かれば pOH を求め、pH が算出できます。
緩衝溶液とpHの保持
溶液のpHは酸や塩基を加えることで変化しますが、酸性成分とその共役塩基(または塩基とその共役酸)を適切な比率で含む溶液は緩衝作用を示し、pH変化を小さく抑えます。緩衝の定量的記述にはヘンダーソン–ハッセルバルヒの式がよく使われます:
pH = pKa + log([A-]/[HA])(対応する酸塩基系に対して)
pHの測定方法
- ガラス電極を用いたpHメータ:最も一般的で定量的。使用前に標準緩衝液で校正(通常pH 4.00、7.00、10.00など)する必要があります。
- 指示薬(リトマス、フェノールフタレインなど)やユニバーサルインジケーター:簡易的に酸性・アルカリ性の有無や大まかなpH範囲を判定するのに有用。
- 比色法や光学測定:研究用途で高精度が必要な場合に用いられることがあります。
測定値は温度やイオン強度、電極の状態に依存するため、正確なpH測定ではこれらを考慮する必要があります。
単位と注意点
pHは「単位を持たない対数量」です(濃度や活性の対数)。そのため「pHの単位」といった表現は誤りです。また、化学実験や工業プロセス、環境・生物関連では温度変化や溶質の種類によりpHの解釈が変わることがあるため、測定条件の明示が重要です。
応用例
- 飲料水や環境水質管理(河川・海水の酸性化の監視)
- 工業プロセス(めっき、化学合成、廃水処理)
- 生体内の酸塩基平衡(血液のpHは厳密に制御されている)
- 食品加工や発酵(pHは微生物の活動や保存性に影響)
最後にまとめると、pHは溶液中の水素イオンの濃度または活性を対数的に示す無次元の指標であり、化学・生物・環境など多くの分野で基本的かつ重要なパラメータです。ほとんどの物質は0から14の範囲のpHを持ちますが、極端な条件ではこれを超える値を取ることがある点に注意してください。アルカリ性の溶液は水素イオンの濃度が低く、代わりに水酸化物イオン(OH-)の濃度が高くなります。
![{\displaystyle {\mbox{pH}}=-\log _{10}\left[{\mbox{H}}^{+}\right]}](https://www.alegsaonline.com/image/093977a79b6a17e02db4699475930e48c05d6468.svg)
![{\displaystyle {\mbox{pH}}=-\log _{10}\left[a_{\mathrm {H^{+}} }\right]}](https://www.alegsaonline.com/image/7a631c4037415f3d4483a6cb07e69858b64890fc.svg)