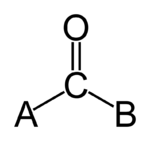
カルボニルとは、分子内のC=O基のことです。これは、炭素と酸素原子の間に二重結合を持つ官能基で、炭素はさらに他に2つの結合を持ちます。これらの結合により、同じカルボニルでも置換基の種類によって性質が大きく変わります。代表例としては、ケトン、アルデヒド、エステルのC=O、カルボン酸、アミド、酸無水物、アシルハライドなどがあります。
構造と電子的性質
酸素は炭素よりも電子陰性なため、結合の電子は酸素の方に偏ります。その結果、カルボニル炭素は部分的に正電荷を帯び、求電子性が強くなります。これがカルボニルの代表的な反応性(求核攻撃を受けやすい)を説明します。一般にカルボニルの炭素・酸素は両方ともsp2ハイブリッドで、平面三角形に近い几何(120°付近)をとります。
- 典型的なC=O結合長は約1.20Å前後で、C–O単結合より短く、C=Cに比べてやや短い。
- 共鳴(O→Cの非共有電子対によるπ共役)により、部分的な単結合性や負電の分配が起きる(アミドなどで顕著)。
- 電子供与基や電子吸引基、共役や環内張力などによって電子密度や結合エネルギーが変わり、これが反応性や分光学的性質に反映される。
主な反応(代表例と反応機構の観点)
カルボニル炭素は求電子的であるため、多くの反応は求核付加や求核的アシル置換を基軸に進行します。主な反応を列挙します。
- 求核付加:ヒドリド(NaBH4, LiAlH4)による還元、グリニャール試薬や有機リチウムによるアルコール生成(付加後のプロトン化で新たな炭素–炭素結合ができる)。
- アルコールとの反応:ヘミアセタール/アセタールの生成(アルデヒド・ケトン+アルコール)。可逆で酸触媒下で進行。
- アミンとの反応:イミンやシュッフ塩基の形成(脱水を伴う)。これを利用した保護や縮合反応が多い。
- 求核的アシル置換:エステル、アミド、酸無水物、アシルハライド間の変換(脱離基の良さに依存)。
- α位化学:α-プロトンの酸性化(エノラート形成)→アルファアルキル化、アルファハロゲン化、アルドール縮合、マイケル付加などの反応へ。
- 縮合反応・C=C生成:ウィッティヒ反応でアルケンへ変換、クロス縮合(アルドール縮合など)。
- 酸化・酸化的反応:アルコールの酸化でカルボニルを生成、Baeyer–Villiger酸化でケトン→エステルへ変換。
反応により新たな不斉中心が生じることが多く、キラル配位子や不斉触媒を用いた不斉合成が盛んに研究されています。
物性と反応性に影響する因子
- 置換基:電子吸引基はカルボニル炭素をより求電子的にし、付加反応を促進する。電子供与基は逆に抑制する。
- 共役:共役系(アルケンや芳香環との共役)はC=Oの電子密度を分散させ、振動数や反応性を変える(一般に求核付加は遅くなることが多い)。
- 立体障害:大きな置換基があると求核攻撃が妨げられる。
- 溶媒・触媒:酸触媒や塩基触媒で反応の経路が変わる(例:酸で加成–脱離が促進、塩基でエノラート形成が促進)。
分光・分析法による同定
カルボニル基は分子内に存在するかどうかを判定しやすい官能基です。代表的な分析法と観察点は次の通りです。
- 赤外分光法では、C=O伸縮振動が非常に強い吸収を示します。一般的にはおおよそ1700 cm−1付近に現れますが、官能基の種類で変化します(例:エステル 1735–1750 cm−1、ケトン ~1715 cm−1、アルデヒド ~1725 cm−1、共役C=Oは低下して ~1680 cm−1、酸無水物は2つのバンド(≈1800, 1750 cm−1)等)。水素結合や共役、置換基の影響でピーク位置が移動します。
- カーボンNMR分光法では、C=Oに対応する13Cシグナルは一般に高い化学シフト(低磁場)領域に現れます。範囲はおおよそ160–220 ppmで、ケトンやアルデヒドは約190–210 ppm、エステルやアミドはやや低い(約160–180 ppm)ことが多いです。これにより他の炭素環境と区別できます。
- 1H NMRでは、アルデヒドのプロトンは約9–10 ppmに現れ、構造のヒントになります。
- 質量分析(MS)では、アシリウムイオンなど特有の断片イオンが観察されることがあり、構造推定に有用です。
自然界での存在と応用
カルボニル基は多くの天然物(糖類、ステロイド、アルカロイドなど)に含まれ、医薬品や農薬、香料、ポリマー材料など工業的にも非常に重要です。カルボニルを介した合成は医薬品合成や天然物合成で中心的な戦略となっています。
実務上の注意点
- カルボニル化合物は空気や水分、酸・塩基に感受性を示すことがあるため、保存や反応条件の選択に注意が必要です。
- 還元や付加反応では選択性(C=Oの選択的還元や不斉制御)を制御するための試薬や触媒が多数存在します。
まとめ:カルボニル基はその電子的性質(酸素への電子偏り)により求核攻撃を受けやすく、合成化学や分析化学で中心的な役割を果たします。構造や置換基、共役などによって性質が大きく変わるため、分光法(赤外分光法では、カーボンNMR分光法では、など)や反応性の理解が重要です。化学反応の設計や物質の同定において、カルボニルは最も扱われる官能基の一つです。