遺伝子治療とは:仕組み・ウイルスベクターとGlyberaの実例解説
遺伝子治療の仕組みを図解で解説―ウイルスベクターの役割と実例Glybera、適応・課題・安全性・将来展望までわかる入門ガイド
遺伝子治療とは、損傷や欠損がある遺伝子の働きを補うために、正常に働く遺伝子を患者の体内に導入する治療法です。目的は、欠損した遺伝子を「修復」することではなく、機能する遺伝子のコピーを供給して症状を改善することにあります。遺伝性疾患だけでなく、がんや一部の代謝疾患など幅広い病態で研究・応用が進められています。
Glybera(実例)の概要と経緯
欧州では、遺伝子治療の中で初期の承認例として注目を集めた製品にGlybera(アルタイプ:alipogene tiparvovec)があります。欧州委員会(欧州医薬品庁の勧告に基づき)はこの製品を一度承認しましたが、承認後の商業的運用上の課題から最終的には販売停止・市場撤退となっています(承認は2012年、事実上の市場撤退は2017年)。Glyberaは家族性リポタンパク質リパーゼ(LPL)欠損症という非常にまれな疾患を対象に設計されました。
Glyberaの仕組み(要点)
- 標的疾患:家族性LPL欠損症。報告頻度は非常に稀で、およそ100万人に1人程度とされることがあります。この病気では脂肪を分解するのに重要なリパーゼ(LPL)の機能が低下し、血液中に中性脂肪(トリグリセリド)が蓄積、繰り返す膵炎(膵臓の痛みや炎症)を引き起こすことがあり、生命に関わる場合もあります。
- ベクター:ウイルスを改変して遺伝子の運搬体(ベクター)とし、機能するLPL遺伝子のコピーを患者の筋肉細胞などに導入しました。Glyberaでは主にAAV(アデノ随伴ウイルス、AAV1サブタイプ)が用いられ、筋肉内に直接注射する方法が採られました。
- 効果:導入された遺伝子が筋肉で発現し、LPL活性が部分的に回復することで血中トリグリセリドが低下し、膵炎の頻度低下が期待されます。
ウイルスベクターと用語の整理
ウイルスを「ベクター」として用いる場合、ウイルスの病原性を取り除き、治療用遺伝子を組み込んで目的の細胞に運ぶ役割を果たさせます。これをウイルスによる遺伝子導入と呼び、専門用語ではトランスダクション(transduction)と言います。記事中にあるトランスフェクションは一般に非ウイルス法(プラスミドや脂質キャリアなど)で細胞に遺伝子を導入する手法を指すため、両者は区別されます。ウイルスベクターを用いる利点は導入効率が高いこと、欠点は免疫反応や長期の安全性に関する問題があることです。
主な種類のベクターと特徴
- AAV(アデノ随伴ウイルス):病原性が低く、非増殖型で主にエピソーマル(細胞核内で独立して存在)に遺伝子を保持するため安全性が比較的高い。ただし容量(運べる遺伝子サイズ)が小さい。
- レンチウイルス(逆転写ウイルス):ゲノムに組み込んで長期発現が期待できるが、挿入による遺伝子変異(挿入変異;insertional mutagenesis)のリスクがある。
- アデノウイルス:高い発現を短期間得られるが、強い免疫反応を引き起こすことがある。
治療法の分類:in vivo と ex vivo
- in vivo:患者の体内に直接ベクターを投与して遺伝子を導入する方法(例:筋肉注射、静脈注射)。Glyberaはin vivo型の代表例です。
- ex vivo:患者の細胞を一度体外に取り出して遺伝子導入を行い、改変した細胞を再び体内に戻す方法。造血幹細胞療法に使われることが多い。
利点と課題(リスク)
- 利点:遺伝子の根本的な原因にアプローチできる、難治性の遺伝性疾患や一部のがんで有効性を示す可能性がある。
- 課題:
- 免疫反応:既存のウイルスに対する抗体があると効果が減弱したり副反応が生じたりする。
- 持続性:AAVのような非統合型では発現が徐々に低下することがある。
- 挿入変異:統合型ベクターではがん化リスクが否定できない場合がある。
- 製造とコスト:高品質のウイルスベクターを大量に製造するのは技術的・経済的に難しく、結果として治療費が非常に高額になりがちです(Glyberaは極めて高価であったことも市場撤退の一因です)。
- 倫理・規制:遺伝子改変の影響範囲や長期安全性について厳しい規制と議論があります。
現在の状況と今後の展望
Glyberaの承認・その後の市場撤退は、遺伝子治療が技術的に可能であっても、臨床上・商業上の課題が大きいことを示しました。一方でその後も研究は進み、網膜疾患に対するLuxturnaや脊髄性筋萎縮症(SMA)に対するZolgensmaなど、有効性と安全性が確認され商用化された例もあります。将来的には、標的性を高め副作用を抑える新しいベクター設計、製造コスト低減、規制の整備が進めば、適応疾患はさらに拡大していくと考えられます。
参考として、この記事で触れた用語や治療の考え方を整理すると、ウイルスをベクターとして用いる技術は強力ですが、ベクターの種類や投与方法により利点とリスクが異なります。ウイルスを用いる治療は一般に「トランスダクション」と呼ばれ、非ウイルス法の「トランスフェクション」とは区別して理解することが重要です。また、遺伝子ノックアウトのような別の遺伝子操作技術とも目的や手法が異なります。
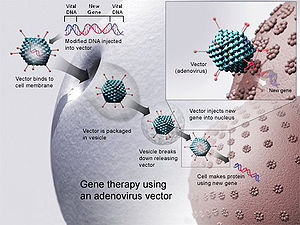
アデノウイルスベクターを用いた遺伝子治療。新しい遺伝子をウイルスに入れて、それを人間に入れて治療します。治療が成功すれば、新しい遺伝子が働く酵素を作り、病気を治療することができます。
中国
中国は、2003年に世界で初めて遺伝子治療の商業生産を承認した国です。その遺伝子治療は、中国で新たに発生するがんの10%を占める頭頸部扁平上皮がん(HNSCC)に対するものです。中国では毎年250万人の新規がん患者が発生しています。
Gendicineという商品名で販売されている、世界初の商業的な遺伝子治療も、ウイルスを使ってヒトのゲノムに遺伝子を挿入するものです。
過去
遺伝子治療の可能性は、DNAとRNAの役割が明らかになると同時に語られるようになった。初めて具体的に発表されたのは1972年のこと。
未来
さらに多くの種類の遺伝子治療が試験段階にあります。今後の臨床医学では、以下のようなサイクルが行われることが明らかになっている。DNAの塩基配列の解析>欠損遺伝子の特定>遺伝子治療や遺伝子ノックアウトによる遺伝子の修正。時には副作用の問題もありますが、それは治験の段階で発見されるかもしれません。現在では、知られているすべての臨床試験をリストアップしたデータベースがあります。
質問と回答
Q: 遺伝子治療とは何ですか?
A: 遺伝子治療とは、患者さんの損傷した遺伝子を置き換えるために、働く遺伝子を挿入するプロセスです。
Q: 欧州委員会はどのような製品を遺伝子治療として承認していますか?
A: 欧州委員会は、遺伝子治療薬として「Glybera」を承認しています。
Q:グリベラはどのように遺伝病を治療するのですか?
A: グリベラは、ウイルスを用いて筋肉細胞に遺伝子のコピーを感染させ、遺伝性疾患を治療します。
Q: リパーゼ遺伝子とは何ですか、またなぜ重要なのですか?
A: リパーゼ遺伝子は、脂肪を分解するために必要な遺伝子です。この遺伝子が損傷していると、血液中に脂肪が蓄積され、生命を脅かす膵炎を引き起こす可能性があるため、重要なのです。
Q:グリベラはどのような手法で遺伝子治療を行っているのですか?
A: グリベラは、ウイルスベクターが遺伝子をヒトの細胞に付着させるトランスフェクション技術を使用しています。
Q: ウイルスベクターとは何ですか?
A: ウイルスベクターとは、遺伝物質を細胞内に運ぶためのキャリアーです。
Q:トランスフェクション法は遺伝子ノックアウト法とどう違うのですか?
A:トランスフェクション法では、ウイルスベクターを用いて遺伝子のコピーを挿入しますが、遺伝子ノックアウト法では、ウイルスベクターを用いません。遺伝子ノックアウト法の目的は、遺伝子を除去または無効にすることです。
百科事典を検索する