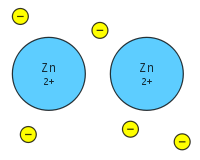
金属結合は、価電子が個々の原子に局在せず、結晶全体にわたって非局在化していることで生じる結合様式です。多くの正のイオン(陽イオン)格子と、その間に広がる自由電子の「海」が相互作用することで物質を一体化します。価電子が原子に強く束縛される共有結合や、明確に陽イオン・陰イオンを作るイオン結合と似ていますが、金属結合では電子が結晶全体を自由に動ける点が大きく異なります。
電子海モデルと仕組み
金属では原子の外側にある電子軌道(原子軌道)同士が重なり合い、電子が個々の原子に縛られずに広がります。これにより電荷を担う電子は特定の原子核に結び付かれず、結晶全体を移動できる「電子海(自由電子)」を形成します。結果として、金属内の電子と正に帯電した原子核(陽イオン)との間に強い静電的な引力が働き、物質にまとまり(凝集力)を与えます。
より詳しくは、個々の原子軌道が多数集まることでエネルギー準位が連続したエネルギーバンドを形成し、そこに電子が占有されるという帯電モデル(バンド理論)で説明できます。バンド内の電子は格子中を容易に移動でき、これが金属の多くの特性の源になります。
金属結合が生む主な性質
- 電気伝導性:自由電子が外部電場に応じて容易に移動するため、金属は良導体になります。電子の移動によって素早く電流を流すことができます。
- 熱伝導性:自由電子がエネルギー(熱)を効率よく運ぶため、金属は熱をよく伝えます(熱伝導)。
- 光沢:自由電子が光を反射することで金属光沢(光沢)が現れます。
- 延性・可鍛性:金属結合は非方向性であるため、原子面が滑りやすく、塑性変形が可能です。これが金属の可鍛性や延性の理由です。
- 高い融点・沸点:自由電子と陽イオン間の強い引力により、一般に融点・沸点が高くなります(ただし例外あり)。この性質は一部でイオン結合と似ています。
- 機械的強度:結晶中の結合による凝集力から、金属は高い強度(強度)を示しますが、結晶構造や不純物の有無で大きく変化します。
例外・特殊なケース
すべての金属が同じ金属結合を示すわけではありません。例えば、水銀は金属結合が比較的弱く、常温で液体となることで知られます。また、遷移金属ではd軌道電子が関与するため、金属結合に部分的な共有結合的性質や磁性が現れることがあります。
さらに、金属以外でも電気を通す物質が存在します。たとえば、黒鉛はπ電子が非局在化しており面内で電気を通します。イオン性化合物は、固体では電気を通さないものが多いですが、溶融や水溶液中では移動可能なイオンによって電流を流します。
合金(合金の定義と種類)
合金は、2種類以上の元素が一体化した金属材料のことで、いわば「金属の溶液」と考えられます。合金化により単一金属では得られない特性(強度の向上、硬さ、耐食性、磁性、導電率の変化など)を実現できます。
主な合金のタイプ:
- 置換型固溶体:原子のサイズや電子数が近い元素が互いの格子位置を置き換えながら混ざる(例:真鍮(黄銅)=Cu–Zn)。
- 間隙型固溶体:小さな原子(例:C、N、H)が金属格子の隙間に入り込む(例:鋼=Fe–C)。
- 化合物的(組織化)合金:特定の組成比で新しい結晶相(準安定または安定)を作る(例:いくつかの高強度合金や耐熱合金)。
合金化は格子歪を生じさせてすべりを妨げるため、強度向上(固溶強化)につながります。一方で、合金成分によっては導電率や延性が低下することもあります。
まとめ
金属結合は、価電子の非局在化(電子海)による非方向性の結合で、これが金属の電気・熱伝導性、光沢、延性・可鍛性、高融点など多くの特性の基盤となっています。ただし、結合の強さや挙動は元素ごと、結晶構造や電子構成(s・p・d電子など)によって異なり、合金化や化学的環境によって性質は大きく変わります。これらの理解は材料設計や金属の用途選択に不可欠です。