トルク選択性とは|電気環状反応の定義、機構と代表例
トルク選択性を図解でわかりやすく解説:電気環状反応の定義・機構・代表例、立体選択性と触媒応用までまとめた入門ガイド
有機化学で、トルク選択性とは、一方の異性体が他方の異性体より多く生成される電気環状反応を指す現象のことです。公式な定義は、「回転性または非回転性の電気環状反応における置換基の内向きまたは外向きの回転を好むこと」と説明されます。言い換えれば、環状化あるいは開環の過程で、環にぶら下がる置換基が反応中に特定の方向へ回転する経路が優先され、その結果として一方の立体異性体が過剰に生じる場合に「トルク選択的」と呼びます。概念は、電子的・立体的要因が回転方向の選択を誘導するという直感に基づき、Kendall N. Houkらによって理論的に整備されました。
基本概念:Woodward–Hoffmann規則との関係
電気環状反応はまず、Woodward–Hoffmannの選択規則に従って同方向回転(conrotatory)か逆方向回転(disrotatory)かが決まります(例:熱的に4n系は同方向回転、4n+2系は逆方向回転が許容される)。トルク選択性はそれに加わる副次的な選択性で、同一の回転モード(同方向または逆方向)内で置換基がどちら向きに回転するか(内向きか外向きか)を決めます。つまり、Woodward–Hoffmannが「どちらの回転モードが許されるか」を示すのに対し、トルク選択性は「その許された回転のうちどちらの方向のトルク(回転方向)を取るか」を決めるものです。
トルク選択性を支配する主な要因
- 立体障害(steric):置換基が内向きに回転すると近接原子と衝突しやすければ、その回転は不利になります。大型基では外向き回転が優勢になることが多いです。
- 電子的要因:電子供与基や電子求引基は、反応遷移状態に生じる部分的な電荷や軌道位相を安定化/不安定化させ、特定の回転方向を有利にします。たとえば、置換基が回転によってπ共役やσ-π相互作用を得られる方向が好まれます。
- 金属錯体やルイス酸の配位:キラルルイス酸やその他の金属錯体が基質に配位すると、電子構造や立体環境が変わりトルク選択性が強く誘導されることがあります(触媒的制御)。この点は合成での不斉化に利用されます。
- 隣接する立体中心やキラル補助基:近傍のキラルセンターがジアステレオ選択的に回転方向を誘導することが多く、その場合トルク選択性はジアステレオ選択性として扱えます。
- 軸-四面体キラリティー移動:軸的キラリティー(例:アレニルやアキシアル配座)から四面体中心へのキラリティー転換が行われる場合、トルク選択性がキラリティー移動の鍵を握ります。
- 温度や溶媒、置換パターン:熱力学的/動力学的要因や溶媒の極性も遷移状態の相対的安定性に影響を与えます。
代表的な反応例と応用
トルク選択性は多数の電気環状反応で観察され、合成化学での立体化学制御に応用されます。典型的な例を挙げると:
- 置換されたシクロブテンの熱的開環(シクロブテン→1,3-ブタジエ):開環中の置換基が内向き/外向きどちらに回転するかで生成するジエンの立体化学が決まる。
- 過環式反応(ペリ環式反応)の一部:置換基の向きが反応座標に沿った回転を選択的に誘導することで、異なる立体配列を与える。
- ナザロフ環化(Nazarov cyclization):特にキラルなアレニルビニルケトンなどを出発物質とした場合、軸-四面体のキラリティー移動を含むトルク選択的な環化により高いエナンチオ選択性が得られる事例が報告されています。置換基や触媒の選択でトルク方向を制御し、単一のエナンチオマーが主生成物となることがあります。
トルク選択性とエナンチオ選択性の関係
環化反応が閉環してキラル中心が生じる場合、トルク選択性はそのままエナンチオ選択性に直結します。環化において許容される回転モードの一方で、回転方向が一方向のみ有利であれば、出発物質から単一のエナンチオマーは、選択的に生成されます。通常、同一回転モードから二つのエナンチオマーが理論的に生じ得るところを、トルク選択性がそれらのうち一方を優先させます。したがって、トルク選択性は可能なエナンチオマー間の非対称誘導(識別)を達成するための重要な概念です。
反応制御と予測
トルク選択性を予測・操作するための一般的な指針:
- 置換基の電子性を検討する:電子供与基はある回転方向で遷移状態を安定化する場合があり、電子求引基は逆方向を好む場合がある。
- 立体障害を評価する:大きな基は内向回転を回避する傾向があるため、外向回転を期待する。
- 触媒や配位の導入:キラルルイス酸や金属触媒を用いることで強い不斉誘導が可能になる。
- 計算化学(例:DFT)の利用:遷移状態エネルギー差を計算することで、どちらの回転がより低エネルギーか予測できる。
研究動向と実践的意義
トルク選択性は単に学術的な興味にとどまらず、天然物合成や不斉合成において高立体選択性を達成するための強力なツールです。理論(Houkらの解析やその後の計算研究)と実験(置換基効果、触媒設計)の両面から研究が進められており、特にナザロフ環化やシクロブテンの開環などで有用な合成戦略が確立されています。近年は、溶媒和や配位効果を含めた高精度計算によってトルク選択性の理解がさらに深まりつつあります。
以上のように、トルク選択性は電気環状反応における重要な副次選択性であり、立体化学の精密制御に寄与します。特に触媒設計や置換基の工夫により、高いエナンチオ選択性やジアステレオ選択性を実現できる点が合成化学上の大きな利点です。実際の応用例としては、キラルなアレニルビニルケトンのトルク選択的なナザロフ環化における軸-四面体キラリティー移動が挙げられます。

アレニルビニルケトンのナザロフ環化反応における軸方向から四面体へのキラリティー移動によるトルク選択性
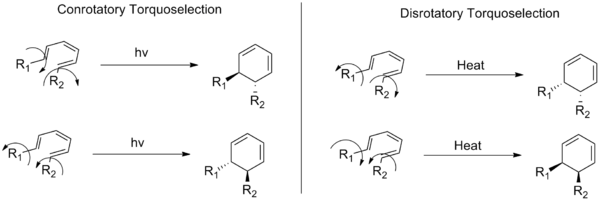
回転の回転モードは、それぞれ、一般的なヘキサトリエン系のエナンチオマーのペアをもたらす2つの可能な回転方向を示しています。注:示されている場合には、反応がトルク選択的である理由はなく、両方の生成物は、どのような特定の条件のセットに対しても期待されます。
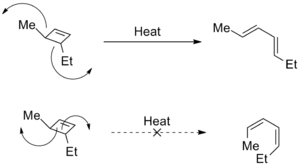
立体ひずみを介して選択性を与えるシクロブテンの熱的電気環状開環反応
質問と回答
Q: トルク選択性とは何ですか?
A: トルク選択性とは、有機化学における現象で、一方の異性体が他方よりも多く生成する電気環反応を表すものである。これは、環状の原子からなる原子団が、反応中に特定の方向に回転する可能性が高い代わりに、両方の可能な方向に回転する可能性が高い場合に起こります。
Q: トルク選択性はジアステレオ選択性とどう違うのですか?
A: トルク選択性は、通常の脂環式反応のジアステレオ選択性とは異なり、Woodward-Hoffmannの法則を超えたものです。ジアステレオ選択性とは、ある立体異性体を他の立体異性体よりも優先することであり、トルク選択性とは、共回転または逆回転の電気環反応において、置換基が内向きまたは外向きに回転することを優先することである。
Q: 化学反応がトルク選択性を持つとはどういうことか?
A: 化学反応にトルク選択性がある場合、1つの回転方向しか許されず(つまり、置換基の回転方向が有利であり)、したがって単一の生成物が得られることを意味します。
Q: この概念はどこから生まれたのですか?
A: torqueselecitivtyの概念は、Kendall N. Houkに由来するものです。
Q: どのような場合に立体的なひずみが選択性をもたらすのか?
A:選択的な電気環反応によって開環する場合、立体歪みが選択性を高める。回転方向が異なると、異なる構造異性体が生成される。
Q: 電子供与性基と電子吸引性基は選択性にどのような影響を与えるのか?
A: 電子供与基や電子吸引基は、反応分子の構造やエネルギーに影響を与えるため、特定の生成物が他の生成物よりも生成されやすく、選択性を変えることができることが研究で示されています。
Q: 電気化学反応以外にトルク活性を伴う機構はあるのか?
A: はい、電気化学反応以外にも、キラルなルイス酸触媒、隣接する立体中心による誘導(この場合、トルクレシオはジアステレオレシオの場合です)、軸から四面体のキラリティ移動(ナザロフ環化反応に見られる)など、トルクレシオを伴うメカニズムがあります。
百科事典を検索する