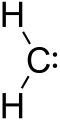カルベンとは、2つの結合を持つ炭素原子と、結合を作らない他の2つの電子を持つ分子のことです。炭素の周りには6個の電子しかないので、かなりの反応性があります。一般式は、R-(C:)-R' と書くことができます。カルベンは中性で電荷を持たない場合と、荷電を帯びたカルベン(カルベニウムやカルベニドなど)がありますが、ここでは中性カルベンを中心に説明します。
定義と電子構造
カルベン中心の炭素原子は通常2つの共有結合を作り、残りの2つの電子は結合していない孤立電子対または単独電子として存在します。カルベンの電子配置は主に2通りに分類されます。すなわち、一重項(singlet)と三重項(triplet)です。
一重項と三重項の性質
カルベンには一重項と三重項がある。第1のタイプでは、結合しない2つの電子は、ローンペアのようなものです。この2つの電子は同じ軌道に留まります。一方、三重項カルベンでは、2つの電子は異なる軌道に留まります。ここでは2つの電子は同じスピンを持っています。
もう少し詳しく言うと:
- 一重項カルベン:2つの電子は対を作って1つの軌道に入り、もう1つの空の軌道(通常はp軌道)を持ちます。スピンは反対向きなので全体のスピンは0です。幾何学的には中心の炭素はsp2様の混成をとり、結合角は比較的曲がった(約120°付近)ことが多いです。電子的には求電子性が強い場合が多く、空のp軌道に求核試薬が攻撃しますが、孤立電子対を持つために求核性を示すこともあります。
- 三重項カルベン:2つの電子は別々の軌道に入り、それぞれが1つずつの孤立電子を持ちます(スピンは平行)。全体のスピンは1(三重項)です。幾何学的には直線に近い配位(より180°に近い)をとることが多く、挙動はラジカルに似ています。水素抽出やラジカル付加などの反応経路を取ることが多いです。
どちらの状態が基底状態になるかは置換基や電子供与/引抜性、共鳴による安定化などに依存します。電子供与性置換基やヘテロ原子による共鳴安定化は一重項を安定化し、アルキル置換などは三重項を好む傾向があります。
代表的な生成方法と検出
- α‑ジアゾ化合物の窒素放出(熱分解、光分解)により生成(R2C=N2 → R2C: + N2)。
- ジアジリンの光分解やトシルヒドラゾンの分解、α‑ハロアルキル化合物のα消失など。
- 金属触媒下での発生(遷移金属カルベン錯体を介して生成する場合)。
カルベンの存在はパルス化学、電子スピン共鳴(ESR)、光学分光、速反応解析などで検出されます。短寿命の自由カルベンはトラップ反応(例えばシクロプロパン化)で間接的に検出されることが多いです。
反応性と主な反応
カルベンは非常に多様な反応を示します。一般的な反応には:
- 二重結合への付加(シクロプロパン化):アルケンに付加してシクロプロパンを与える。求電子剤的な挙動(軌道相互作用)や、三重項の場合はラジカル付加の段階を経ることもあります。
- C–H挿入:飽和炭化水素のC–H結合に挿入して新たなC–C結合を作る。
- 付加–開環や再配置反応:例えばウルフ再配置(Wolff rearrangement)など。
- 求核・求電子両性:一重項は空のp軌道のため求電子性を示しやすいが、孤立電子対を持つため求核性を示す場合もある。三重項はラジカル様の反応(H抽出、ラジカル付加)を示す。
- ヤリド生成:カルベンがホスフィンや硫黄化合物と反応してヤリドを形成することがある。
また、カルベンに類似する「カルベノイド(carbenoid)」と呼ばれる中間体(例えばSimmons–Smith反応でのジオモンZincカーベノイド)は、自由カルベンと異なり金属に結合して反応性を制御します。
触媒応用と安定化されたカルベン
ほとんどのカルベンは非常に不安定ですが、近年は安定化された(いわゆる「持続性」または「安定」)カルベンが合成され、広く応用されています。特に重要なのはN‑ヘテロ環式カルベン(NHC)で、窒素原子による共鳴・σ供与によりカルベン中心が安定化されます。これらは単離可能で、金属錯体の強力な配位子や有機触媒(有機触媒、ルイス塩基触媒)として用いられます。
遷移金属と結合したカルベン錯体は触媒化学で非常に重要です。例えばルイス・アクロス的な性質の“Fischer型”カルベン(遅元素、π受容性配位子を伴う)や、より求核的な“Schrock型”カルベン(初期遷移金属、酸化数の高いもの)などがあり、触媒反応の機構や反応性に応じて使い分けられます。代表的な応用例としてはオレフィンの縮重結合(メタセシス)触媒として知られる、ロバート・グラブスらが開発したグラブス触媒のように、金属‑カルベン中間体を鍵として働くものがあります。
実験上の注意とまとめ
カルベンは一般に高い反応性を持つため、生成と同時に他の分子と反応してしまうことが多いです。そのため実験的には低温、光条件、または金属錯体や安定化基で制御して取り扱います。短寿命のカルベンはトラップ試薬を用いて間接的に検出・同定するのが普通です。
まとめると、カルベンは「二価の炭素中心に孤立電子が2個存在する中性種」であり、一重項・三重項という2種類の電子状態を取り得ます。反応性は非常に多様で、合成化学や触媒化学で重要な役割を果たします。特に安定化されたカルベン(NHCなど)や遷移金属カルベン錯体は、実用的な触媒および配位子として広く用いられています。