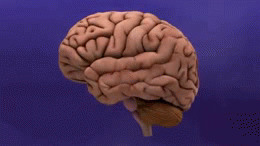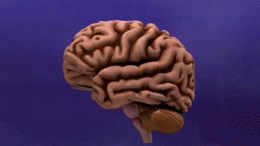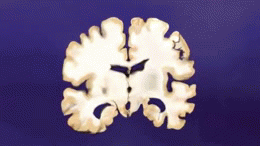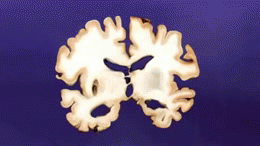
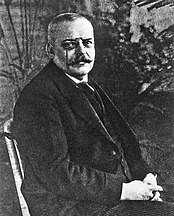アルツハイマー病(AD)は、脳の細胞がゆっくりと破壊されていく脳の病気です。時間の経過とともに記憶や思考、言語、行動などに影響を及ぼし、日常生活が難しくなります。現在のところ完全な根治療法はありませんが、症状を緩和したり進行を遅らせたりする治療法や介入が存在します。アルツハイマー病は高齢者に多く見られる病気ですが、これは通常の老化の一部ではなく、病的な変化です。老人性認知症の中で最も多いタイプで、全認知症の約60~80%を占めるとされています。
主な症状
アルツハイマー病の症状はゆっくり進行します。代表的な症状には次のようなものがあります。
- 短期記憶の低下(最近の出来事を忘れる、同じことを繰り返し質問する)
- 言葉が出にくくなる、名前が思い出せない
- 判断力・計画力の低下(お金の管理や約束を守るのが困難になる)
- 場所や時間の見当識障害(道に迷いやすくなる)
- 性格・行動の変化(無関心、抑うつ、不安、易怒性など)
- 日常生活動作の低下(着替え、食事、入浴などの介助が必要になる)
初期には軽度認知障害(MCI)の形で現れることがあり、その後ゆっくりと認知症へ進行することがあります。
病因(原因)と危険因子
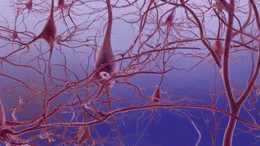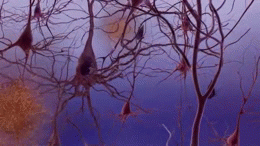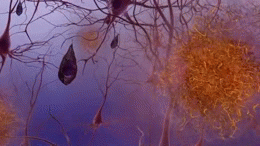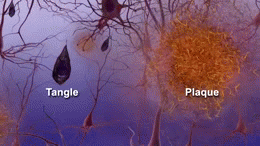
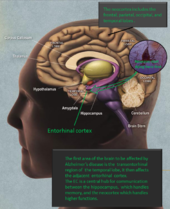
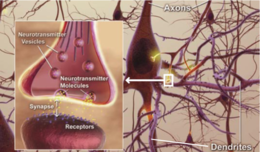
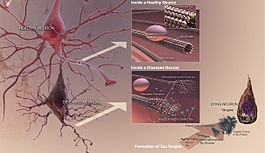
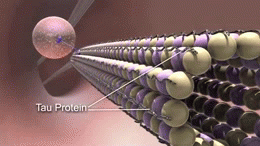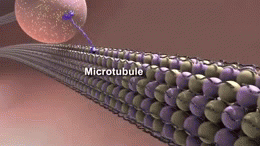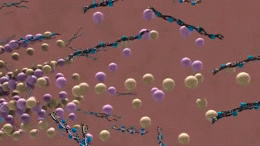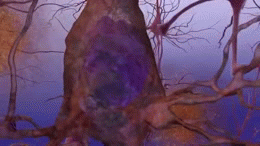
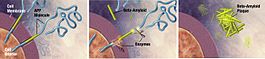
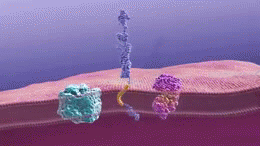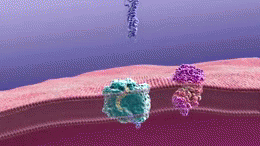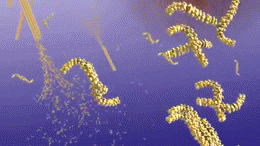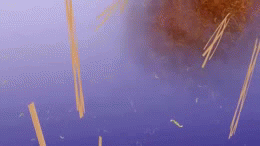
アルツハイマー病の正確な原因はまだ完全には解明されていませんが、脳内にアミロイドβ(Aβ)プラークやタウ(tau)タンパクの異常蓄積が生じ、神経細胞や神経回路の破壊を招くことが主要メカニズムとして考えられています。また、炎症や血管障害、代謝異常なども関与していると見られます。
アルツハイマー病の原因はまだ正確には知られていないが、人がアルツハイマー病になる可能性が高くなる危険因子がいくつかある。
- 年齢:最大のリスク因子。65歳以上で発症率が上昇します。
- 遺伝的要因:家族性の早発型アルツハイマーにはAPP、PSEN1、PSEN2変異が関与します。遺伝的リスクを高める一方、最も一般的なリスク遺伝子はAPOE ε4です。
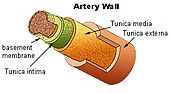
- 血管リスク:高血圧、糖尿病、高脂血症、喫煙などは認知症リスクを高めます。
- 生活習慣:運動不足、社交性の低下、聴力障害、睡眠障害などがリスクに関連するとの報告があります。
診断
診断は医師による問診、神経心理学的検査(MMSEやMoCAなど)、身体診察、血液検査で他疾患を除外することから始まります。必要に応じて次の検査が行われます。
- 脳MRIやCT:萎縮パターンや血管性変化の評価
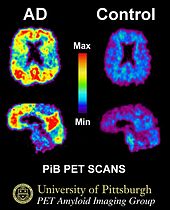
- PET検査(アミロイドPET、タウPET):病理マーカーの可視化
- 脳脊髄液(CSF)検査:Aβ、総タウ、リン酸化タウの測定
- 血中バイオマーカー:近年は血漿中のp-tauなど有望な検査が実用化されつつあります
- 遺伝学的検査:家族性の早発例では遺伝子検査を行うことがあります
早期診断は適切な治療・介護計画や将来の意思決定に役立ちます。気になる症状があれば早めに専門医に相談してください。
治療とケア
現在の治療は主に症状の改善と進行の遅延を目的としたものです。薬物療法と非薬物療法を組み合わせて行います。
- 薬物療法(症状緩和):コリンエステラーゼ阻害薬(ドネペジル(日本名:ドネペジル塩酸塩)、リバスチグミン、ガランタミン)やNMDA受容体拮抗薬(メマンチン)が認知機能や日常生活能力の維持に用いられます。
- 疾患修飾療法(研究・一部承認薬):脳内アミロイドを標的とする抗体治療(アデュカヌマブ、レカネマブなど)は一部の国で承認・臨床導入されていますが、有効性と安全性、適応基準について議論が続いており、出血や脳浮腫(ARIA)などの副作用に注意が必要です。
- 非薬物療法:認知リハビリテーション、作業療法、音楽療法、運動療法、環境調整や行動療法が日常生活の質を向上させます。
- ケアとサポート:介護者教育、支援サービス、法的・金銭的な準備、緩和ケアの導入など総合的な支援が重要です。
治療は患者さんの状態や病期に合わせて個別化されます。主治医や専門チームとよく相談してください。
早期発見と予防
早期発見は治療や生活設計に有利です。次のような変化に気づいたら受診を検討してください:物忘れが日常生活に影響する、約束を忘れる、道に迷うことが増えた、言葉が出にくくなる、性格の変化など。
また、生活習慣の改善は発症リスクの低下や進行の遅延につながる可能性があります。具体的な対策は次のとおりです。
- 定期的な有酸素運動(週に中強度の運動を目安に)
- バランスのとれた食事(地中海食やMIND食が有益とする研究あり)
- 高血圧、糖尿病、脂質異常症などの循環器リスク管理
- 禁煙、節度ある飲酒
- 十分な睡眠、聴力の補完(補聴器の使用)
- 社会的交流や生涯学習、認知刺激活動
また、病気の発症を遅らせるために役立つ可能性のある生活習慣について、医療専門家と相談しながら取り組むことが推奨されます。
疫学と経過
年齢とともに有病率は増加します。たとえば「現在65歳の人がアルツハイマー病にかかるリスクは10.5%と推定されている」といった報告や、アルツハイマー病がアメリカでは第6位の死因であるというデータもあります。以前の推計では2007年時点で全世界で2,660万人以上の患者がいるとされていましたが、近年の推定では2020年時点で認知症患者は約5,500万人と報告され、今後さらに増加する見込みです(人口高齢化に伴う増加が要因)。
進行速度や経過は個人差が大きく、数年から十年以上にわたることがあります。早期診断と包括的な介入により、患者さんのQOL(生活の質)を保つことができます。
歴史的背景
この病名は、ドイツの精神科医で神経病理学者のアロイス・アルツハイマーが、1906年にフランクフルトの病院で診た中年女性の症例(オーギュスト・デターのケース)を詳細に報告したことに由来します。後にアルツハイマーの共同研究者であるエミール・クラエペリンが「アルツハイマー病」と名付けました。
最後に、疑わしい症状がある場合は早めに医療機関で評価を受けることをおすすめします。治療や介護の選択肢、支援制度は年々進歩していますので、専門医と連携して最適なケアを検討してください。

-MRI.png)