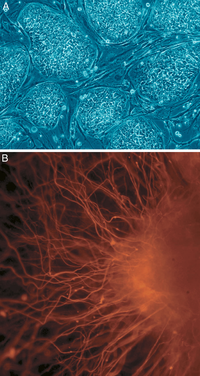
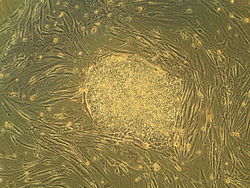
幹細胞とは、分裂して分化することができる体の細胞(体細胞)のことです。つまり、自己複製(同じ性質の細胞を作り続けること)と、別の種類の細胞へと変化する能力(分化)という二つの重要な性質を持っています。
幹細胞の基本的な性質
- 自己複製(self‑renewal):長期間にわたり同じ性質の細胞を作り続ける能力。
- 分化能(potency):どの程度多様な細胞に分化できるかを示す概念。代表的な区分は以下のとおりです。
- 全能(totipotent):受精卵のように個体全体を形成できる能力(胚葉・胚外組織すべて)。
- 多能(pluripotent):胚性組織のほぼすべてに分化可能(胚性幹細胞やiPS細胞など)。
- 多能性より狭い多能性(multipotent):血液や皮膚のように特定系統の複数の細胞に分化する能力(成体幹細胞など)。
- 単能(unipotent):一種類の細胞へ分化する能力。
- ニッチ(微小環境)依存性:幹細胞は体内で与えられた環境(シグナル、支持細胞、細胞外マトリックス)によって挙動が決まります。
種類と代表例
哺乳類の幹細胞には、大きく分けて胚性幹細胞と成体組織に存在する成体幹細胞の2種類があります。これに加え、近年は体細胞を人工的に初期化して作る誘導多能性幹細胞(iPS細胞)も重要です。
- 胚性幹細胞(ES細胞):胚(初期胚)から取り出され、多くの細胞種に分化できる多能性を持つ。
- 成体幹細胞:骨髄の造血幹細胞、皮膚や腸管の幹細胞、神経系の幹細胞など、各組織に存在してその組織の恒常性や修復を担う。成体では、幹細胞は体の修復システムとして機能し、特殊な細胞を補充するだけでなく、血液、皮膚、腸管組織の正常なターンオーバーを維持しています。
- 誘導多能性幹細胞(iPS細胞):成熟した体細胞に特定の因子を導入して初期化し、多能性を取り戻した細胞。患者由来細胞を用いることで免疫拒絶の課題を小さくする可能性があります。
入手源(採取場所)と培養
幹細胞は体内のさまざまな場所や臍帯血、骨髄などから採取できます。本文中にもあるように、臍帯血や骨髄を含む様々な供給源から、高度に可塑性のある成人幹細胞を採取することができます。組織培養で増殖させ、適切な条件下では筋肉や神経などの特殊な細胞に形質転換(分化誘導)することも可能です。
臨床応用と実績
- 造血幹細胞移植:白血病や悪性リンパ腫などに対する骨髄移植・臍帯血移植は最も確立された幹細胞治療です。
- 組織再生医療の試み:角膜上皮や皮膚の再生、心筋や神経の再生を目指した臨床試験が進行中です。iPS細胞由来細胞を用いた網膜疾患や心疾患への応用は臨床段階に入ってきています。
- 免疫調節と細胞療法:間葉系幹細胞(MSC)は免疫抑制・抗炎症作用が期待され、移植片対宿主病(GVHD)などで利用されています(研究段階や臨床試験が中心)。
最新の研究トピック(概略)
- iPS細胞と臨床応用の進展:患者由来のiPS細胞から作った細胞を用いた安全性・有効性試験が進んでいます。
- 臨床用幹細胞の品質改良:遺伝子編集(CRISPR等)による病因修正、細胞拡大薬剤(例:HSC拡大因子)を使った供給量改善など。
- オルガノイド・3D培養:臓器様のミニ組織(オルガノイド)を幹細胞から作り、病態解析や創薬スクリーニングへ応用。
- 単一細胞解析とニッチの理解:single‑cell解析で幹細胞の多様性や分化経路、微小環境の役割が詳細に解明されつつあります。
- 直接リプログラミング:ある体細胞を一度多能性に戻すことなく直接別の細胞へ転換する技術の研究。
課題と倫理・安全性
- 腫瘍化リスク:特に多能性細胞(ES/iPS由来)では未分化細胞が残ると腫瘍を形成する危険があるため、分化誘導と除去が重要です。
- 免疫拒絶:他人由来の細胞移植では免疫抑制や適合性の問題が発生します。患者由来iPSの利用やHLAハプロタイプバンクの整備が検討されています。
- 倫理的配慮:胚性幹細胞の取得やヒトの胚操作には倫理的議論が伴います。各国で規制とガイドラインが整備されています。
- 未承認治療に対する注意:有効性・安全性が確立していない幹細胞治療を標榜するクリニックが存在し、被害報告もあるため、科学的根拠と規制に基づいた治療を選ぶことが重要です。
実用的なポイント(患者・一般向け)
- 幹細胞研究は急速に進んでいるが、多くの治療はまだ臨床試験段階であり、すべてが実用化されているわけではありません。
- 治療を検討する際は、治験情報や担当医による説明、倫理審査と規制(厚生労働省や各国の規制機関)を確認してください。
- 臍帯血などの保存を検討する場合は、長期保存の実績や費用・利用可能性を比較検討しましょう。
まとめると、幹細胞は自己複製と分化能という特性により、基礎生物学から再生医療、創薬まで幅広い応用が期待される一方で、技術的・倫理的な課題も残されています。現在も世界中で基礎研究と臨床研究が併進しており、将来的に多くの疾患治療の選択肢になる可能性があります。