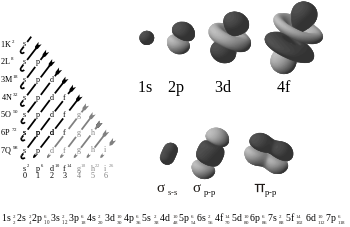
化学では、π結合(π結合)とは、一方の電子の軌道の軌道が他方の電子の軌道と交差(重なり)してできる共有結合の一種を指します。具体的には、p軌道のように核を中心に2つのローブをもち、ローブ間に結節面(ノード面)をもつ原子軌道同士が側面で重なり合うことで生じます。重なり合う領域は通常2つあり、軌道の位相が同じ領域では結合性の電子密度が増加します。軌道の結節面のうちの1つだけが、関与する核の両方を通過する、という性質が特徴です。
その名前のギリシャ文字πはp軌道を指し、π結合の軌道対称性は結合軸を軸に見下ろしたときにp軌道同士の側面重なりと同じ形に見えることから由来します。通常、p軌道同士の側面重なりでπ結合が形成されます。d軌道も理論的にはπ様の重なりを取ることが可能で、超原子価や一部の金属錯体において重要となる場合がありますが、実際の化学結合でのd軌道の直接的寄与は系によって大きく異なります。
パイ結合は通常、シグマ結合よりも弱い結合です。これは、量子力学は、軌道の重なり積分(オーバーラップ積分)に依存することを示しており、p軌道同士は側面で平行に並ぶためσ結合を作る軸方向の重なりに比べて重なりが小さいためです。その結果、同じ原子間距離で比較すると、σ結合が最も強く、π結合はそれより弱くなります。
π結合は、2つの原子軌道が重なり合う2つの領域を介して接触したときに起こります。π結合は、シグマ結合よりも広がりのある結合であり、π結合に存在する電子は一般にπ電子と呼ばれます。π結合で結合した分子断片は、π結合を壊さずにその結合について自由に回転することはできません。回転しようとすると、平行だった2つのp軌道の位相関係が崩れ、π結合が失われるためエネルギー的に不利になります。
結合次数と多重結合
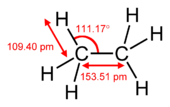
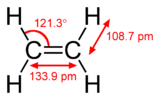
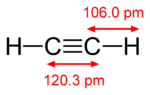
π結合はσ結合と組み合わさって多重結合を作ります。二重結合は一般に1つのσ結合と1つのπ結合、三重結合は1つのσ結合と2つのπ結合(互いに直交するp軌道同士の重なりから生じる)で構成されます。各π結合は結合次数を1だけ増加させ、結合エネルギーと結合長に影響します。例えばC=C二重結合はC–C単結合より短く、C≡C三重結合はさらに短く強いです。
π結合と非局在化(共役)
隣接する複数のπ結合や不対電子、または非共有電子対が重なり合うと、電子は分子全体にわたって非局在化(共役)します。共役により系全体の電子状態が安定化し、吸収スペクトル(UV–Vis)に特徴的な遷移が現れたり、化学反応性や酸化還元特性が変化したりします。共役環が環状で4n+2個のπ電子を満たす場合は芳香族性を示し、特に高い安定化を受けます(例:ベンゼン)。
π結合の力学的・化学的影響
- 回転障壁:π結合は分子の回転を制限し、幾何異性(シス・トランス) を生じさせます。
- 反応性:π電子はσ結合よりも外側に存在するため求電子反応や付加反応、酸化反応の標的になりやすいです。ラジカルやカチオンなどを安定化する場合もあります。
- 分光学的指標:C=Cの伸縮振動は赤外領域で約1600 cm−1付近、UV–Visでは共役系により波長が長波長側へシフトします。NMRではアルケニック(vinylic)プロトンが芳香族や飽和プロトンより低磁場(下方シフト)に現れます。
π結合の分子軌道的見方
分子軌道(MO)理論では、原子軌道の結合性および反結合性線形結合からπ結合性(π)軌道とπ*(パイスター)反結合性軌道が生じます。π電子はしばしば分子のHOMO(最高被占軌道)として振る舞い、化学反応において重要な役割を果たします。π*はLUMO(最低空軌道)として求電子反応の受け入れ側となることが多いです。
重原子でのπ結合とd軌道の関与
第三周期以降の元素(例えばS, P, Clなど)や遷移金属では、d軌道が形状・エネルギーの点でπ相互作用に関与することがあります。金属錯体ではリガンドから金属へのπ供与や金属からリガンドへのπ逆供与(π-backbonding)が重要で、これによりCOなどの結合強度や振動数が変化します。一方で、超原子価化合物における"d軌道参加"は古典的説明の一部であったものの、現代の計算化学では電子の再配置や3中心2電子・3中心4電子結合など他のモデルで説明される場合も多いことに注意が必要です。
まとめ
π結合はp軌道などの側面重なりによって生じる共有結合で、σ結合に比べて重なりが小さいため一般に弱いものの、分子の構造、回転制限、反応性、光学的・電子的性質に大きな影響を与えます。多重結合・共役・芳香族性・金属との相互作用など多様な化学現象の基盤として非常に重要です。