RNAスプライシングとは|定義と仕組み、スプライセオソームによるエクソン結合と機能・生物学的意義
RNAスプライシングの定義と仕組みをわかりやすく解説 スプライセオソームによるイントロン除去とエクソン結合で最終mRNAが作られる過程と生物学的意義を詳述
RNAスプライシングは、遺伝子転写の後に行われる重要なRNA加工過程です。DNAの塩基配列情報はまずプレmRNAとして転写され、そのプレmRNAから翻訳に適した成熟したメッセンジャーRNA(mRNA)が作られます。最終的にできたこのメッセンジャーRNAは、翻訳によって正しいタンパク質を合成するための鋳型として使われます。
定義と基本的な流れ
分子生物学的には、スプライシングとは、前駆体mRNA(プレmRNA)中の非コード領域であるイントロンを切り出し、残ったコード領域であるエクソンを連結して連続した配列にするプロセスを指します。これによって最終的な機能的mRNAが形成されます。なぜこの過程が必要かというと、多くの真核生物の遺伝子は、遺伝子が複数のエクソンとイントロンに分かれているためです。
スプライシングの仕組み(分子レベル)
スプライシングは酵素反応というよりは、RNAによる触媒活性を含む複合体的な切断・連結反応で、2回の転位反応(トランスエステリフィケーション)で進行します。一般的な配列要素としては以下が知られています。
- 5'スプライス部位(多くの場合「GU」から始まる配列)
- ブランチポイント(ほとんどの場合保存されたアデニン塩基)
- ポリピリミジン(ピリミジン塩基が富む領域)トラック
- 3'スプライス部位(多くの場合「AG」で終わる配列)
これらの配列シグナルを認識して正確にイントロンを除去し、エクソンをつなぎ合わせることで読み枠が維持されたmRNAが生成されます。
スプライセオソームの構成と組み立て
イントロン除去の化学反応は主にリボ核タンパク質複合体であるスプライセオソームによって触媒されます。スプライセオソームは小核リボ核タンパク質(snRNP、例えばU1、U2、U4、U5、U6)と多数のタンパク質因子から構成されます。スプライセオソームの組み立ては段階的で、一般に次のような過程を経ます(E→A→B→B*→C複合体):
- U1 snRNPが5'スプライス部位に結合
- ブランチポイントにU2 snRNPが結合してA複合体形成
- U4/U5/U6トリプレックスが加入してB複合体へ移行
- 構造変化とsnRNA間の再配置により触媒活性を持つC複合体が形成され、連続する2つの切断・結合反応(トランスエステリフィケーション)が起きる
これらの反応によりイントロンはラリアット(枝状構造)となって切り出され、エクソン同士が連結されます。
選択的スプライシング(オルタナティブスプライシング)
多くの真核生物では、同じ遺伝子から複数のmRNAアイソフォームが作られることがあり、これを選択的スプライシングまたはオルタナティブスプライシングと呼びます。代表的なパターンは次の通りです:
- エクソンのスキッピング(あるエクソンが取り除かれる)
- イントロン保持(通常は除去されるイントロンが残る)
- 代替5'または3'スプライス部位の使用
- 相互排他的エクソン(同じ位置で片方のエクソンしか使われない)
オルタナティブスプライシングは組織特異的、発生段階特異的、シグナル応答性などにより柔軟に制御され、タンパク質の多様性と機能変化を生み出します。
スプライシングの調節
スプライシングは配列要素だけでなく、多数のタンパク質因子によって調節されます。代表的な調節因子には、SRタンパク質(スプライシング促進因子)やhnRNP(スプライシング抑制因子)があり、エクソン近傍やイントロン内のエンハンサー/サイレンサー配列に結合してスプライシング部位の選択を助けたり阻害したりします。さらに、転写とスプライシングは時間的・空間的に連携しており、RNAポリメラーゼの速度やクロマチン状態もスプライシング結果に影響します(共転写的スプライシング)。
生物学的意義と疾患との関連
スプライシングは単にイントロンを取り除くだけでなく、次のような重要な生物学的役割を持ちます:
- タンパク質バリエーションの創出による機能多様性の確保
- 組織・発生段階特異的な遺伝子発現の調節
- 翻訳効率やmRNAの局在、安定性の制御
一方で、スプライシング異常は多くの疾病と関連します。例えば、スプライシング制御因子やスプライス部位の変異は遺伝性疾患やがんの原因となることが知られています。有名な治療例としては、スプライシングを標的としたアンチセンスオリゴヌクレオチド療法(例:SMA治療薬のnusinersen)があり、特定のエクソンの利用を変えることで病態を改善します。
研究手法と応用
スプライシングの研究には以下のような手法が用いられます:
- RT-PCRやqPCR:特定転写産物のアイソフォーム解析
- RNAシーケンシング(RNA-seq):全転写物の網羅的解析とオルタナティブスプライシングの検出
- ミニジーンアッセイや遺伝子編集技術:スプライシング要素の機能解析
- 抗体や化学的阻害剤を用いたスプライセオソーム因子の研究
これらの知見は基礎生物学だけでなく診断や治療法開発にも応用されています。例えば、スプライシング異常を標的にした薬剤やオリゴヌクレオチドは臨床応用が進んでいます。
まとめ
要するに、スプライシングはプレmRNAから機能的なmRNAを生成するために不可欠なプロセスであり、スプライセオソームを中心に高度に制御されています。イントロンの除去とエクソンの結合は遺伝子発現の多様性を生み出し、正常な発生や細胞機能の維持に重要です。同時に、その異常はさまざまな疾患と結びつくため、分子レベルでの理解と応用(診断・治療)は現代バイオメディカル研究の重要課題となっています。
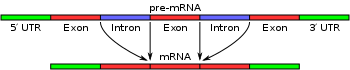
プレmRNAのエクソンとイントロン、およびスプライシングによる成熟mRNAの形成を簡単に図示したもの。UTRは、mRNAの末端にあるエクソンの非コード部分。
代替スプライシング
多くの場合、スプライシングプロセスでは、同じメッセンジャーRNAのエクソンの構成を変化させることによって、さまざまなユニークなタンパク質が作られます。この現象を代替スプライシングと呼びます。代替スプライシングには様々な方法があります。エクソンを伸ばしたり、スキップしたり、イントロンを残したりすることができる。
真核生物と原核生物の比較
スプライシングは、生命のすべての王国や領域で行われていますが、スプライシングの範囲や種類は、主要な部門間で大きく異なる場合があります。真核生物は、多くのタンパク質をコードするメッセンジャーRNAといくつかのノンコーディングRNAをスプライシングする。一方、原核生物はほとんどスプライシングを行いません。もう一つの重要な違いは、原核生物にはスプライソソームが存在しないことである。
ディスカバリー
フィリップ・シャープとリチャード・ロバーツは、イントロンとスプライシングプロセスの発見により、1993年にノーベル生理学・医学賞を受賞した。
1977年、シャープ研究所とロバーツ研究所の研究により、高等生物の遺伝子はDNA分子に沿って複数の異なるセグメントに分かれている「スプリット」であることが明らかになった。
遺伝子のコード領域は、タンパク質の発現に関与しない非コードDNAによって分離されている。非コード領域であるイントロンは、シャープが「スプライシング」と呼ぶプロセスで前駆体mRNAから切り離される。分割された遺伝子構造は、ほとんどの真核生物の遺伝子に共通していることがわかった。
質問と回答
Q: RNAスプライシングとは何ですか?
A: RNAスプライシングとは、プレmRNAのイントロンを取り除き、エクソンを結合して、タンパク質の生産に使われる最終mRNAを作るプロセスのことです。
Q: RNAスプライシングの目的は何ですか?
A: RNAスプライシングの目的は、イントロンと呼ばれる非コード部分を取り除き、エクソンと呼ばれるコード部分を結合して、タンパク質の生産に使用できる最終的なmRNAを作成することです。
Q: メッセンジャーRNAとは何ですか?
A: メッセンジャーRNA(mRNA)とは、DNAからタンパク質に遺伝暗号を伝達するRNAの一種です。
Q: メッセンジャーRNAを作るには、何段階あるのですか?
A: メッセンジャーRNAを作るには、2つの段階があります。
Q: メッセンジャーRNAの構築の第一段階では何が起こるのですか?
A: メッセンジャーRNAの構築の第一段階では、各遺伝子がプレmRNAに翻訳されます。
Q: スプライセオソームとは何ですか?
A: プレmRNA中のイントロンを取り除き、エキソンを結合するRNAスプライシングを行う細胞内の機械です。
Q: メッセンジャーRNAから正しいタンパク質はどのように作られるのですか?
A: 正しいタンパク質は、メッセンジャーRNAから、mRNAの遺伝暗号を使ってアミノ酸を組み立ててタンパク質にする翻訳というプロセスによって作られます。
百科事典を検索する