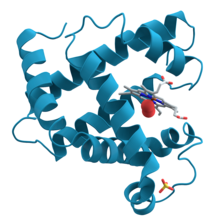
タンパク質は、アミノ酸という小さな単位からなる長鎖の分子である。これらのアミノ酸は互いにペプチド結合で連結され、一本の鎖(ポリペプチド)を形成することが基本形である。化学的性質や配列の違いにより、ポリペプチドは特定の立体構造をとり、その立体構造がタンパク質の機能を決定する。
1つまたは複数のポリペプチドが円形または繊維状に折り畳まれた生化学的な化合物である。ポリペプチド鎖がどのように折りたたまれるかは、鎖中のアミノ酸の性質(疎水性・親水性、電荷、分岐など)や、鎖間・鎖内で形成される水素結合、イオン結合、疎水相互作用、ジスルフィド結合などの化学的相互作用によって決まる。
構造の階層
- 一次構造:ポリペプチドを構成するアミノ酸の直線配列。配列は遺伝情報に由来する(下記)。
- 二次構造:αヘリックスやβシートなど、局所的に安定した規則的な折りたたみ。
- 三次構造:ポリペプチド全体がとる立体構造。複数の二次構造要素の相互配置として記述される。
- 四次構造:複数のポリペプチド鎖(サブユニット)が集合してできる複合体(例:ヘモグロビンは複数サブユニットから成る)。
アミノ酸配列と遺伝情報
ポリペプチドとは、アミノ酸の一本鎖のポリマーである。ポリペプチドを構成するアミノ酸の配列は、遺伝子のDNA配列に由来する。遺伝情報は転写・翻訳の過程を経てタンパク質配列へと変換され、遺伝暗号によって20種類の標準アミノ酸が指定される。さらに翻訳後に起こる化学的な修飾(リン酸化、糖鎖付加、メチル化、アセチル化など)はタンパク質の折りたたみ、安定性、局在、活性、および機能を大きく変化させる。
立体構造の安定化要因と折りたたみ過程
タンパク質の立体構造は、次のような相互作用で安定化される:
- 水素結合(主鎖・側鎖間)
- 疎水相互作用(疎水性残基の集合)
- イオン結合(塩橋)や静電相互作用
- ジスルフィド結合(システイン残基間の共有結合)
- 金属イオンや補因子との配位結合
タンパク質はしばしば翻訳と同時か翻訳直後に正しい立体構造へ折りたたまれるが、複雑な折りたたみにはシャペロン(分子シャペロン)と呼ばれる補助因子が必要になることがある。誤って折り畳まれたタンパク質は凝集を起こし、細胞障害や変性疾患(例:アルツハイマー病やプリオン病)を引き起こすことがある。
補助因子と翻訳後修飾
合成直後に、いくつかのアミノ酸は化学的に修飾される。これにより、タンパク質の折りたたみ、安定性、活性、および機能が変化する。タンパク質には、補酵素として、ペプチド以外の基(ビタミン由来の補因子や金属イオン)が付いていることがあります。これらの補因子は触媒活性や電子移動、基質結合に必須であることが多い。
生物学的機能
細胞内外でのタンパク質の役割は非常に多岐にわたる。主な機能を挙げると:
- 酵素:化学反応の触媒として働く
- 構造タンパク質:細胞骨格や組織の構造を保持する(例:コラーゲン、アクチン)
- 輸送・貯蔵:酸素運搬(ヘモグロビン)、イオンや分子の輸送(例:チャネル、トランスポーター)
- シグナル伝達:受容体やホルモン、二次メッセンジャーの制御に関与
- 免疫応答:抗体や補体系の構成要素として病原体を認識・中和
- 運動:モータータンパク質(例:ミオシン、キネシン)による力の発生と輸送
ほかにも翻訳因子や転写因子、細胞周期制御因子など、ほぼすべての細胞プロセスにタンパク質が関与している。これは、他の生体高分子(多糖類や核酸)と同様に、タンパク質が細胞の機能的基盤を成しているためである。
研究法と応用
タンパク質の構造や機能を調べる代表的な方法には次がある:X線結晶構造解析、核磁気共鳴(NMR)、クライオ電子顕微鏡(cryo-EM)、質量分析など。バイオインフォマティクスを用いた配列解析や構造予測(例:αFoldなどの計算法)も急速に発展している。これらは創薬、酵素設計、バイオテクノロジー分野で重要な役割を果たす。
まとめ
タンパク質は、アミノ酸の配列に基づいて折りたたまれ、多様な立体構造と機能を持つ生体分子である。遺伝子情報から合成され、翻訳後の修飾や補因子により機能が多様化する。正しい折りたたみとその調節は生命活動にとって不可欠であり、その理解は医学・バイオテクノロジーにおける応用に直結する。