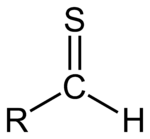
チオアルデヒド(略してチアル)は一般式 RC(S)H をもつ化合物の総称です。基がRC(S)Hであるすべての分子を指す。チオアルデヒドは、アルデヒドの酸素原子を硫黄に置き換えたような分子であり、硫黄は炭素に二重結合を持ちます。硫黄原子は 2 つの 孤立ペアを保持し、酸素を含むカルボニル(C=O)とは異なる電子密度分布と立体特性を示します。
基本的な性質
- 電子的性質:チオカルボニル(C=S)結合は酸素を含むカルボニル(C=O)に比べてπ結合の重なりが弱く、硫黄はより多極化しやすいため、炭素原子は強い親電子物質となります。
- 反応性:チオアルデヒドは非常に反応性が高く、自立状態ではしばしば自己反応(重合・縮合・付加)を起こします。単独で安定に存在することは稀です。
- 光学・分光特性:C=S の振動は赤外吸収帯で特徴的に現れ、ラマン分光で強く出ることがあります(C=O とは波数域が異なる)。NMR でもチオカルボニル周辺の化学シフトは酸素系カルボニルとは異なる傾向を示します。
- 臭気・取り扱い:多くの硫黄含有化合物と同様に悪臭を示すことがあるため、取扱いは換気や密閉容器、低温条件下で行うのが望ましいです。
代表的な反応性
- 求核攻撃:チオアルデヒドの炭素は強い求電子性を示すため、アルコール、アミン、チオールなどの求核剤が付加してヘミチオアセタールやヘミチオアセタール類似体を形成することがあります。
- 自己反応・重合:生成直後に二量化・重合しやすく、安定体として単離するのが難しい例が多いです。
- 付加環化反応:チオアルデヒドは良好なジエンフィレ(あるいは一般的な付加剤)として振る舞い、例えばディールス-アルダー反応も進行しやすいことが知られています。その他の環化反応や六員環、硫黄含有ヘテロ環の前駆体として有用です。
- 酸化還元:チオカルボニルは酸化や還元により性質を変えやすく、例えばチオアルデヒドの酸化で二硫化物や酸化硫黄生成物が生じる場合があります。
安定化と合成法
- 置換基による安定化:生成した瞬間に自己反応する性質を抑えるため、嵩高い(立体的に大きな)R基を導入するとチオアルデヒドはより安定になります。原子団が大きいことで近接反応が抑えられます。
- チオケトンとの比較:すでに述べたように、H を他の R 基で置換するとチオケトンと呼ばれる分子(一般式 R2C=S)になり、チオアルデヒドより一般に熱力学的に安定です。
- 保護・誘導体化:不安定なチオアルデヒドは、二量化の抑制や取り扱いの容易化を目的に金属錯体化、チオアセタール化(dithioacetal)やジチオラン化などの形で保護されることがあります。
- 合成法:典型的には既存のカルボニル化合物を硫黄置換試薬(Lawesson 試薬や P4S10 など)でチオン化(O→S 変換)する方法や、求核的にチオカルボニルを導入する特殊な合成経路が用いられます。多くの場合、チオアルデヒドは反応中間体として生成され、低温や不活性雰囲気下で捕捉・反応させます。
実例と応用
- 芳香族基をもつチオアルデヒド(例:チオベンザルデヒド類)は、ジエンとの付加反応やヘテロ環合成の有用な出発物質となります。
- 単純なチオホルムアルデヒド類は非常に不安定で、気相中や低温でのみ観測されることが多く、溶液中では二量化・重合してしまいます。
- 有機合成では一時的な中間体として利用されることが多く、特殊な付加反応や環化反応を介した分子構築に活用されます。
取り扱い上の注意
- 多くは不安定かつ反応性が高いため、発生させたらすぐに消費する(in situ 生成・利用)か、十分に安定化してから扱うことが推奨されます。
- 硫黄化合物特有の臭気や毒性を伴う場合があるので、換気、有機溶媒の適切な管理、保護具の着用を行ってください。
まとめると、チオアルデヒド(チアル)は構造的にはアルデヒドの酸素を硫黄に置き換えたもので、強い親電子性と高い反応性を示します。安定化には立体障害や置換基の工夫、保護・錯体化などが有効であり、実際には多くの合成反応で中間体として、または特殊な合成戦略の要素として重要な役割を果たします。