環化付加反応とは、二重結合が環構造に置き換わった反応物間の化学反応である。それは、"2つ以上の不飽和分子(または同じ分子の一部)が結合して、結合の多重度が正味で減少する環状付加物を形成する "周期の化学反応である。環化反応である:原子の新しい環を作る。
環化付加反応は、結合される分子の基本的な大きさによって名前が付けられます。このため、Diels-Alder反応は[4 + 2]環化付加反応となり、1,3-双極性環化付加反応は[3 + 2]環化付加反応となります。このような反応は非極性付加反応である。
基本的な定義と特徴
- 定義:二つ以上の不飽和結合を持つ部位が結びつき、新しい環を形成する付加反応。表記は「[m + n]」で表され、結びつく原子数に基づく。
- 生成物:生成物では結合の多重度(例えば二重結合の数)が正味で減少する。
- 分類:主に「ペリシクリック(同時に結合が作られる協奏的反応)」と「段階的(ラジカルやイオン中間体を経る)」に分かれる。
主な種類と代表例
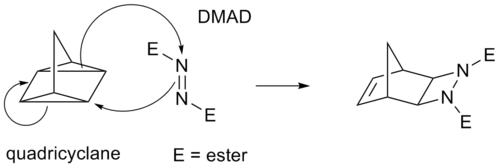
- [4+2] 環化付加(Diels–Alder反応)
- シクロヘキサン骨格を与える典型的な例で、熱的に進行することが多く、一般に協奏的(同時に2本の結合ができる)な反応です。
- 立体化学が保存されやすく、endo則(副軌道相互作用による選択性)を示す場合があります。
- Diels-Alder反応は天然物合成や医薬品合成で非常に重要です。
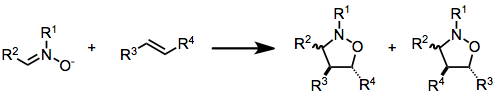
- [3+2] 環化付加(1,3-双極子環化)
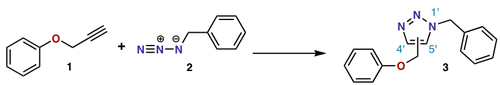
- アジドやニトロンなどの1,3-双極子とアルケンやアルキンが反応して五員環を作ります(ヒューズゲン反応など)。
- 近年の代表例に「銅触媒によるアジド-アルキン環化(CuAAC、“クリック化学”)」があります(機構は金属触媒下で段階的な経路を取ることが多い)。
- [2+2] 環化付加
- 熱条件では対称性の制約で禁止されることが多いが、光照射(励起状態)下では進行します(光化学的に許容)。
反応機構と軌道対称性(Woodward–Hoffmann則)
- 多くの環化付加反応はペリシクリック反応であり、分子軌道の位相保存が反応の可否と立体化学を決めます。これはWoodward–Hoffmannの軌道対称性則で説明されます。
- 協奏的(同時)経路:全ての結合形成が単一遷移状態を通る(例:標準的なDiels–Alder反応)。この場合、suprafacial(同じ面から結合)やantarafacial(反対面から結合)などの位相様式が重要です。
- 段階的経路:ラジカルやイオン中間体を経由するもの。金属触媒や光反応でよく観察されます。
立体化学・配向性(選択性)の予測
- 立体選択性:反応が協奏的な場合、基質の立体置換は生成物の立体配置にそのまま反映されることが多い(立体保存性)。
- 配向性(レジオ選択性):分子軌道(HOMO/LUMO)のエネルギー差と局在度に基づいて予測されます。電子供与基と電子求引基の位置関係が重要です(正規電子需要型 vs 逆電子需要型)。
- エンド対エクソ選択:Diels–Alder反応ではエンド生成物が熱力学的あるいは遷移状態の安定性により優先されることがある(副軌道相互作用の影響)。
反応条件と触媒
- 加熱、光照射、酸や塩基、金属触媒(Cu, Pd, Rhなど)、ルイス酸(AlCl3, BF3, SnCl4など)が用いられます。
- ルイス酸はジエンやジエノフィルのLUMOを下げて反応性を上げ、反応速度と選択性を改善することが多いです(特にDiels–Alder)。
- 光化学条件は[2+2]反応など、熱では禁止される反応を可能にします。金属触媒は段階的機構を経由して高い化学選択性を与えます(例:CuAAC)。
代表的な応用例
- 天然物合成:複雑な環状骨格を一挙に構築するために多用されます(例:ステロイドやアルカロイドの合成ステップ)。
- 医薬品合成:環形成により複雑性を早期に導入できるため有用です。
- 材料化学:ポリマー合成や機能性分子の構築(光反応やクリック化学)に応用されます。
- 生体化学的応用:生体分子の修飾や生体内での結合形成を目的としたバイオコンジュゲーション(例:アジド-アルキン“クリック”反応)。
注意点と例外
- 全ての環化付加反応が協奏的ではありません。機構を誤認すると、予想と異なる立体・配向性を生むことがあります。
- [2+2]の熱反応禁止則、光化学的許容性など、軌道対称性に由来する制約を常に考慮する必要があります。
まとめ
環化付加反応は、有機合成で非常に強力なツールです。反応の表記([m+n])、機構(協奏的か段階的か)、軌道対称性、触媒や条件を理解することで、目的の環や立体化学を効率よく構築できます。実際の設計ではFMO理論や既知の置換効果、触媒の作用を総合的に考慮してください。
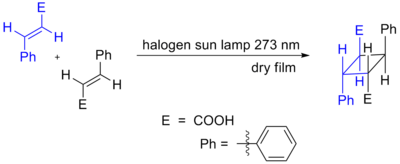
.png)
![Intermolecular Formal [3+3] Cycloaddition Reaction](https://www.alegsaonline.com/image/600px-3+3-cycloaddition.svg.png)