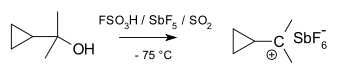
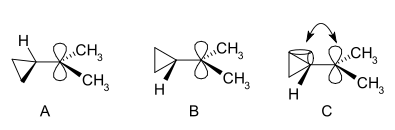
カルボカチオンとは、正電荷を持つ炭素原子を持つイオンのことである。荷電しているその炭素原子は、通常の中性炭素が持つ8個の価電子(オクテットルール)に対して6個の価電子しか持っていないため不安定で、電子を受け取って安定化しようとする。カルボカチオンは化学反応の中で重要な中間体として振る舞い、他の分子から電子(電子対)を受け取ることで中性に戻る。
構造と電子配置
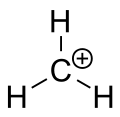
古典的・単純化した説明では、カルボカチオンの正電荷は空の軌道に由来するとされ、時にsp3混成を伴うと説明されることがある。しかし、より正確には多くの典型的なカルボカチオンはsp2混成を取り、三つのsp2軌道で3本のσ結合(または2本のσ結合+孤立電子対)を作り、残った1つの垂直方向のp軌道は空である。この空のp軌道は基準面に対して垂直で、分子骨格は概ね平面(三角形)に近い構造を示すため、求電子(負電荷を与える電子対)やヌクレオフィルがこの空軌道に攻撃して結合を再生する。
安定性に影響する要因
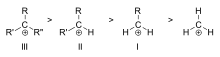
- アルキル置換効果(ハイパー共役):アルキル基は隣接するC–H結合を通じて空のp軌道と共役し、電子を部分的に分散させカルボカチオンを安定化する。一般に、置換が多いほど(メチル→一次→二次→三級)安定性が高い。
- 共鳴(共役)安定化:ベンジル カルボカチオンやアリル カルボカチオンのように、正電荷が複数の原子に分散できる場合、非常に安定になる。共鳴はアルキル置換による安定化より強力なことが多い。
- 電子引寄/電子供与置換基:電子を供与する基(例:-OR, -NR2)は正電荷を安定化し、電子を引く基(例:-NO2)は不安定化する。
- 誘起効果と溶媒和:極性溶媒や配位能のある溶媒(例:水、アルコール)はカルボカチオンを溶媒分子で安定化できる。反応速度や中間体の寿命に影響する。
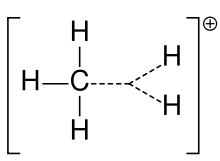
- 非古典的・架橋カルボカチオン:2-ノルボルニル陽イオンなど、一部の系では正電荷が一つの炭素に局在せず橋状に分散する「非古典的」構造を取り、これが安定化に寄与する。
分類と代表例
- アルキルカルボカチオン:メチル、一次、二次、三級(一般に三級が最も安定)。
- アリルカルボカチオン:CH2=CH–CH+ のように二重結合に隣接する場合、共鳴で安定化。
- ベンジルカルボカチオン:フェニル基に隣接する正電荷はベンゼン環への共鳴で強く安定化される。
- 芳香族陽イオン(例:トロピリウムイオン):環状系で6π電子の芳香性を持つ場合、非常に安定で独立したイオンとして存在しうる。
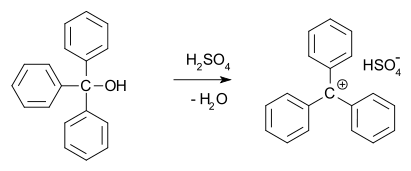
- トリフェニルメチル陽イオン(トリチル陽イオン):置換基が多く電子供与的な芳香族環で取り囲まれているため、安定で単離された塩が得られることもある。
生成方法と関与する反応
- ヘテロリシス(C–X結合の切断):ハロゲン化アルキルの溶媒和分解(SN1)で中間的に形成。
- 付加–脱離反応(E1脱離):脱離によって発生し、その後脱プロトン化してアルケン生成に進む。
- アルケンのプロトン化:アルケンに酸が付加すると、カルボカチオンが生成されることがある(マルコフニコフ則に基づく付加反応など)。
- 水素・アルキル抽出(ハイドリド・メチル移動):反応中により安定なカルボカチオンを形成するための再配置(ハイドリドシフト、メチルシフト)が頻繁に起こる。
反応性と機構上の重要性
カルボカチオンは強い求電子種であり、ヌクレオフィルによる捕捉(付加)や、溶媒・陰イオンによる安定化、または再配置を通じて反応経路を決定づける。SN1型置換反応やE1型脱離反応ではカルボカチオンが鍵となる中間体であり、その安定性が反応速度や生成物の分布を大きく左右する。
観測・実験的証拠
- 低温NMR:安定化されたカルボカチオンは低温条件で検出されることがある(例:トリフェニルメチル陽イオンの観測)。
- 色とUV/可視吸収:共役系で安定化された陽イオンは色を示すことがあり、紫外可視分光で特徴的な吸収を持つ。
- 塩としての単離:超弱配位陰イオン(例:SbF6–, BF4–、カルボランアニオンなど)を伴う塩として単離・結晶化される例がある。
- 質量分析・反応速度論:反応中間体としての存在は速度論的データや質量分析断片から支持される。
重要な注意点(ポイント)
- 安定性の一般順序:三級(3°)> 二次(2°)> 一次(1°)> メチル(ただし共鳴やその他の効果により例外あり)。
- 再配置が起こりやすい:より安定なカルボカチオンを形成するためにハイドリドシフトやアルキルシフトが起こるため、生成物予測では再配置を常に考慮する必要がある。
- 非古典イオンの存在:全てのカルボカチオンが単純に一原子に正電荷が局在するわけではない。系によっては架橋構造や分極した共鳴構造をとる。
まとめると、カルボカチオンは有機反応の中で非常に重要な求電子中間体であり、その構造(主にsp2混成・平面構造)、安定化要因(ハイパー共役、共鳴、溶媒効果など)、および再配置の可能性を理解することが、反応機構の予測と制御に不可欠である。