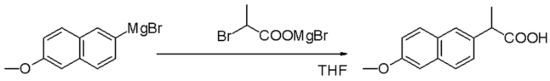
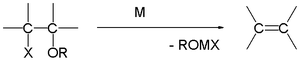
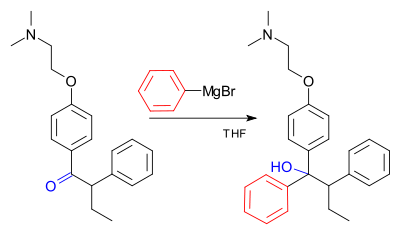
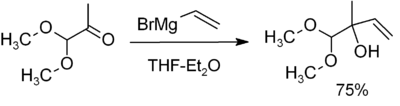グリニャール反応(発音: /ɡriːˈɲɑːr/)は、有機金属化学反応の一種で、アルキルまたはアリールマグネシウムハライド(グリニャール試薬、一般式 RMgX)が、酸素や窒素などに結合した電気的に求電子的な炭素原子を攻撃して新しい炭素–炭素結合を形成する反応です。典型的にはカルボニル化合物(アルデヒド、ケトン、エステル、酸クロリドなど)への求核付加として進行し、付加後の加水分解によりアルコール類やカルボン酸誘導体が得られます。グリニャール反応は有機合成における最も基本的で重要なC–C結合形成法の一つです。
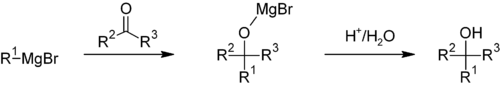
機構(概略)
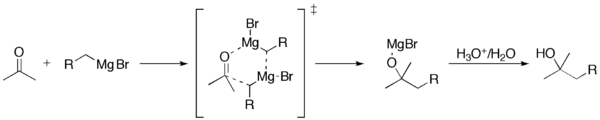
- グリニャール試薬は炭素からマグネシウムへ部分的に負の電荷を持つとみなせる求核種で、極性結合によって部分的に正電荷を帯びた炭素(例:カルボニル炭素)を攻撃します。
- カルボニルに付加すると、酸素上にマグネシウム塩化物で安定化されたアルコキシド中間体が生成します。続く水や酸での加水分解によりアルコールが得られます。
- エステルや酸クロリドの場合は、反応が2回進行して第三級アルコールが得られることが多く、ニトリルとは付加後の加水分解でケトンが得られます。
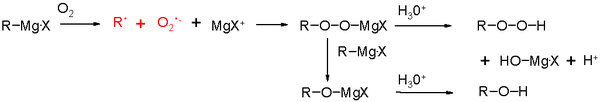
- 付加反応は一般に求核付加(ニュークレオフィリック・アタック)として説明されますが、実際には溶液中でRMgXは集合体や錯体を形成し、電子移動過程や多体反応が関与することもあります。
試薬の性質と反応性
- 強塩基性・強求核性:アルキル基の共役酸(対応するアルカン)のpKaは非常に高く(概ね ~45–50)ため、グリニャール試薬は強塩基であり、酸性プロトンを持つ基質(例:水、アルコール、カルボン酸、アミンの一部)とは即座に不活性化してしまいます。
- 配位と集合体:溶媒として用いられるエーテル類(エーテル、THFなど)がマグネシウムに配位して錯形成し、溶媒和されたクラスターとして存在します。従って「イオン性ではない」という表現は、完全な自由イオンではなく集合体・錯体として振る舞うことを示します。
- 官能基の互換性:ニトロ基、酸、アルコール、アミン、有機酸塩などの酸性または還元されやすい官能基は共存できません。酸化・求電子性の高い基とも副反応を起こします。
- ハロゲン化アルキルとの反応:SN2機構で他のハロゲン化アルキルと直接反応して安定にC–C結合を作ることは一般に困難です。ハロゲン化アルキルとグリニャール試薬の混合は電子移動やラジカル過程、あるいは副反応(Wurtz様の結合形成)を引き起こすことがあり、望ましい収率で単純なSN2的結合形成が起きにくいためです。
生成法と取り扱い上の注意
- 代表的な製法は、乾燥した溶媒中でマグネシウム金属にハロゲン化アルキル(R–X)を作用させる方法です。反応開始のために微量のヨウ素や2,2′-ジブロモジフェニル、加熱、超音波などでマグネシウム表面を活性化することがあります(例:超音波を使ってマグネシウムの表面を活性化)。
- 溶媒はエーテル類(ジエチルエーテル、THFなど)が用いられます。これらはマグネシウムと配位して試薬を安定化させます。
- 水分・酸素に敏感であり、微量の水でも試薬はプロトン化されて失活します。反応器具は火炎乾燥や真空置換で乾燥させ、反応は不活性ガス雰囲気(窒素・アルゴン)下で行うのが通常です。反応溶媒や溶質の前処理(乾燥)も重要です。
- 安全面:強い還元性・可燃性があり、空気中の水や酸に触れると発熱・発火・ガス発生を起こすことがあるため慎重な取り扱いが求められます。
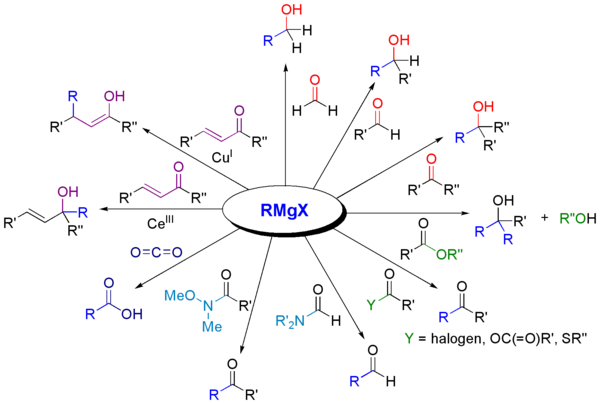
代表的な応用例
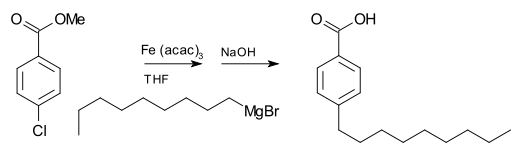
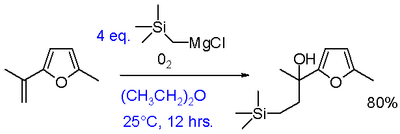
- カルボニル化合物への付加による一次・二次・三次アルコールの合成。
- 二酸化炭素との反応でカルボン酸を与える(R–MgX + CO2 → RCO2MgX → 酸性加水分解 → RCO2H)。
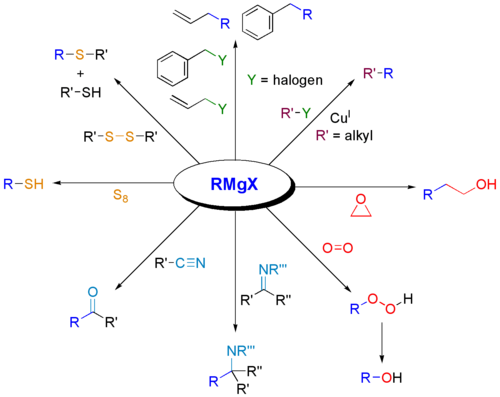
- ニトリルとの反応後加水分解でケトンを合成。
- エポキシ化合物への求核開環(末端の攻撃によりアルコールを伴う付加)。
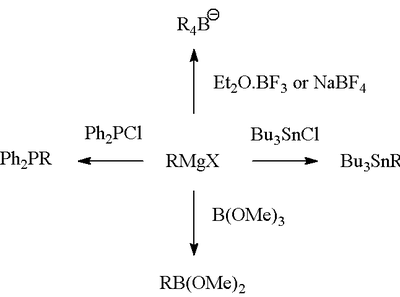
- 前駆体として他の有機金属(ボロン化、ケイ素化、スズ化など)への変換を経てクロスカップリング反応に用いるなど、複合的な合成戦略の一部として利用されます(炭素–リン、炭素–スズ、炭素–ケイ素、炭素–ボロン結合構築への応用)。
問題点と対処法
- 水や酸性プロトンによる失活:徹底した乾燥・不活性雰囲気の維持が必要。
- ハロゲン化アルキル同士の直接的なC–C結合形成が難しい点:求核置換が成立しにくいため、代替法(有機銅試薬やカップリング法)を用いることが多い。
- 試薬の活性化や収率向上には、金属表面の処理(洗浄、超音波、微量ヨウ素添加など)や高純度溶媒の使用が有効です。
歴史
グリニャール試薬および反応はフランソワ・オーギュスト・ヴィクトル・グリニャール(François Auguste Victor Grignard)が発見し、この業績により彼は1912年にノーベル化学賞を受賞しました。以後、有機合成化学において不可欠な手法として広く用いられています。
まとめ:グリニャール反応は強力なC–C結合形成反応であり、高い合成的価値を持つ一方で、水や酸性官能基に非常に敏感であるため、適切な取り扱いや保護基戦略を必要とします。用途に応じた溶媒・条件の選択と安全管理が重要です。