ジンクフィンガーヌクレアーゼ(ZFN)とは?遺伝子編集の定義・仕組みと用途
注目の遺伝子編集技術ジンクフィンガーヌクレアーゼ(ZFN)とは?定義から仕組み、医療・研究での用途やリスクをわかりやすく解説。
ジンクフィンガーヌクレアーゼ(またはZFN)は、遺伝子を標的にしてDNAを変化させるための人工的な酵素(ヌクレアーゼ)です。これは、人工ヌクレアーゼを用いてゲノムを改変する方法の一つで、特定の配列を認識して二本鎖切断(DSB:double‑strand break)を導くことで、細胞内のDNA修復機構を利用して遺伝子を改変します。
ZFNは大きく分けて二つの部分で構成されています。ひとつはDNA配列を認識するモジュールであるジンクフィンガー、もうひとつはDNAを切断する核酸分解酵素ドメインです。ジンクフィンガーは亜鉛イオンを含む小さなタンパク質ドメインで、通常1つのジンクフィンガーが約3塩基対の配列を認識します。複数のジンクフィンガーを連結することで、より長く特異的な配列を標的にすることができます。切断ドメインには一般にFokIの制限酵素由来ドメインが用いられ、これは単独では切断活性を示さず、2つのモノマーが隣接して結合しドメインが二量体化することで切断を行います。したがって、ZFNは通常「左右一対」で設計され、互いに向かい合って結合したときにターゲット領域の間のスペーサー配列で二本鎖切断を生じます。
作用の仕組み(簡単な流れ)
- 設計:目的の標的配列に結合するようにジンクフィンガーを組み合わせ、左右一組のZFNを設計する。
- 結合:各ZFNモノマーがそれぞれの側の配列に結合する。
- 切断:FokIドメインが二量体化して二本鎖切断を生じる。
- 修復:細胞のDNA修復機構が働き、DNA修復により変化が導かれる。主に非相同末端結合(NHEJ)または相同組換え修復(HDR)が起こる。
生じる変化の種類
ZFNによる二本鎖切断の結果、修復過程で以下のような変化が生じます。
- 欠失(deletion)や挿入(insertion):NHEJでは誤って塩基欠損や挿入が入り、しばしばフレームシフト等による遺伝子欠失(ノックアウト)が得られます。
- 正確な置換や挿入(ノックイン):HDRを利用して、供与体(ドナー)DNAをテンプレートに用いると、狙った塩基置換や遺伝子の挿入が可能です。
主な用途
- 基礎研究:特定の遺伝子の機能解析のためにノックアウトや変異導入を行う。遺伝学の研究で頻用される。
- 医療応用(研究・臨床試験):遺伝疾患の遺伝子修復や免疫細胞改変(例えばT細胞の受容体改変やCCR5の改変など)など、主に外因性に取り出した細胞を編集して再移植するex vivo療法で検討されてきた。
- 農業・家畜改良:耐病性・耐環境性の向上や形質改変を目的としたゲノム改変。
- 産業バイオテクノロジー:微生物や細胞株の性能向上(代謝経路の最適化など)。
導入・送達方法
ZFNを標的細胞に届ける方法にはいくつかあり、用途によって使い分けられます。代表的な方法:
- ウイルスベクター(AAV、レンチウイルスなど)を用いた遺伝子導入
- mRNAやプラスミドによる一過性発現
- タンパク質(RNP:リボヌクレオプロテイン)として直接導入(エレクトロポレーションなど)
利点と限界・リスク
利点
- 特異的に設計すれば高い標的性が期待できる。
- ex vivo治療の臨床応用に向けたノウハウが蓄積されている。
限界・リスク
- ジンクフィンガー配列の設計・最適化が技術的に難しく、時間と費用がかかる。
- オフターゲット(非標的部位)での切断や過剰な二本鎖切断による細胞毒性のリスクがある。
- HDR依存の正確な改変は細胞種や細胞周期に依存し効率が低い場合が多い。
安全性向上の工夫
- FokIドメインを「義務的ヘテロ二量体化(obligate heterodimer)」型に改変し、ホモ二量体による非特異的切断を低減する。
- オフターゲット検出技術の進展により、設計段階での評価を厳格化する。
- 一過性発現やタンパク質導入(RNP)により、切断活性を短時間に限定して安全性を高める。
他のゲノム編集技術との比較
TALENやCRISPR/Cas9と比較すると、ZFNは長年にわたり実用化が進められてきましたが、設計の難しさやコスト面でCRISPRに比べて不利とされることが多いです。一方で、特定の状況ではZFNのほうがオフターゲットが少ない、あるいは既存の臨床データが豊富であるといった利点もあります。
歴史と臨床展開
ジンクフィンガー技術は1990年代から開発が進み、ZFNを用いた研究・臨床試験がその後行われてきました。臨床試験では主に免疫細胞や造血幹細胞を一度体外で編集して再導入するex vivoアプローチが採られ、安全性や有効性の評価が進められています。
今後の展望
ZFNは設計や安全性改善の研究が続けられており、オフターゲット低減や効率向上のためのタンパク質工学が進展しています。CRISPRなど新しい技術と役割を分担しつつ、特定の応用分野ではZFNが引き続き有用なツールであり続ける可能性があります。
総じて、ジンクフィンガーヌクレアーゼは高い標的特異性を目指した古典的かつ実用的なゲノム編集技術の一つであり、用途に応じた適切な設計と安全性評価が重要です。
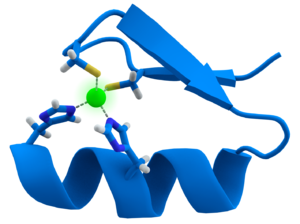
ジンクフィンガー分子の3D表示。ジンクフィンガーは青、亜鉛イオンは緑のラベルが貼られている。
ジンクフィンガー構造
ジンクフィンガー」は、多くのタンパク質構造の名前です。亜鉛原子がタンパク質を結合して、より安定したものにしています。ZFNはDNAの塩基対に結合します。1つのジンクフィンガーは、それだけで約3つの塩基対を結合することができます。
ZFN機能
ジンクフィンガーヌクレアーゼは、3~6本の亜鉛フィンガーで作られています。ZFNには、DNA結合ドメインとDNA切断ドメインという2つの重要なドメインがあります。DNA切断ドメインでは、Foklという酵素を使ってDNAを切断します。
ZFNは、自分が設計したDNA配列のみを変化させることができます。DNA結合ドメインは、特定のDNA配列に結合します。同じDNA配列用に設計された2つのZFNが1つの遺伝子を変更する必要がある。DNA結合ドメインは、DNA二重らせんの両鎖に結合する。DNA切断ドメインは、DNA鎖を切断し、遺伝子の塩基対を切り出す。細胞は、DNA修復機能を使って、壊れたDNA鎖を自分で修復する。DNA修復後に塩基対が欠落すると、欠失型の突然変異が生じる。
ターゲット遺伝子配列の長さを指定することもできます。3本のジンクフィンガーを使って、最小9塩基対の変更が可能です。これは、非常に短いDNA配列を除去・挿入して、ターゲット遺伝子への影響を調べるのに便利です。また、2本以上のジンクフィンガーを使って、大きな配列を変更することも可能です。
ZFNの使用について
ZFNは、多くの遺伝学的研究において、遺伝子の機能を発見するために使用されています。ZFNは、あらゆる種のDNAを変化させるために使うことができます。ZFNのもう一つの特徴は、in vivo(生体内)で使用できることです。現在は、植物、昆虫、魚などのモデル生物に使われています。
ZFN遺伝子改変の研究に関わる生物のリストは以下の通りです。
ZFNの問題点
ZFNの最大の問題は、標的遺伝子以外の遺伝子を誤って改変してしまうことです。ZFNは、標的遺伝子上の正しい塩基対を見つけるように作られなければなりません。この塩基対は、標的遺伝子だけが持つように選ばれます。DNA切断ドメインはどんなDNA配列にも作用するので、間違った遺伝子配列に結合すると、代わりにその遺伝子を変えてしまいます。2つ以上の遺伝子の塩基対をノックアウトするZFNは正確ではないと考えられます。
質問と回答
Q: ジンクフィンガー・ヌクレアーゼ(ZFN)とは何ですか?
A: ジンクフィンガー・ヌクレアーゼ(ZFN)は遺伝子を標的としてDNAを変化させるために使用されるツールです。
Q:操作されたヌクレアーゼを用いてゲノムを変化させる3つの方法とは何ですか?
A: ジンクフィンガーヌクレアーゼ(ZFN)、Transcription Activator-Like Effector Nucleases(TALEN)、Clustered Regularly Interspaced Short Palindromic Repeats(CRISPR)の3つが、人工ヌクレアーゼでゲノムを変化させる方法です。
Q: ジンクフィンガーとは何ですか?
A: ジンクフィンガーは、特定のDNAに結合するタンパク質と亜鉛からなる人工分子です。
Q:ジンクフィンガーヌクレアーゼ(ZFN)とは何ですか?
A:亜鉛フィンガーヌクレアーゼ(ZFN)は、亜鉛フィンガーとフォクルと呼ばれるDNA切断酵素を融合させた酵素です。
Q: ZFNが特定のDNA配列に結合するとどうなりますか?
A:ZFNが特定のDNA配列に結合すると、そのDNA配列を2ヶ所で切断します。
Q: DNAが切り取られた後、通常の細胞酵素は何をするのですか?
A: 通常の細胞酵素は、切り取った部分を除いた末端をくっつけます(DNA修復)。
Q: ジンクフィンガーヌクレアーゼまたはZFNができる2種類のDNA変化とは何ですか?
A: ジンクフィンガーヌクレアーゼまたはZFNは2種類のDNA変化を起こすことができます。
百科事典を検索する