化学では、分子軌道(MO)とは、分子内で原子が結合したときに電子に何が起こるかを説明するものです。MOは、分子内の電子の波動的な振る舞いを説明する数学的な関数です。化学者は、化学的・物理的性質を予測したり説明したりするために、このような関数を使用します。例えば、この関数は、ある特定の領域に電子が見つかる確率を教えてくれます。
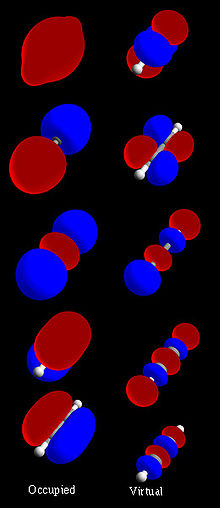
化学者は通常、原子軌道を組み合わせて分子軌道の数学モデルを構築します。また、分子の各原子からのハイブリッド軌道や、原子のグループからの他の分子軌道を使うこともできます。コンピュータはこれらの機能を扱うことができる。分子軌道は、化学者が量子力学を応用して分子を研究することを可能にします。分子軌道は、分子の原子がどのようにくっついているかについての質問に答えます。軌道図の様々な丸みを帯びた形は、原子のどこに電子があるかを示しています。
基本概念:分子軌道とは何か
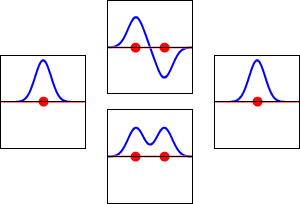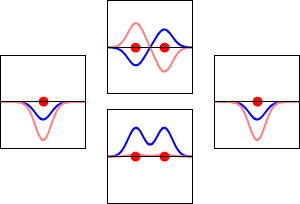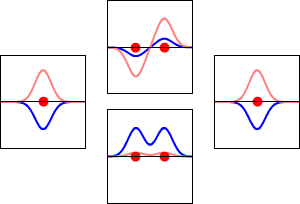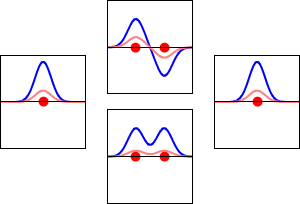
分子軌道(MO)は、分子全体に広がる電子の存在確率を表す波動関数の一部で、通常は「一電子軌道」として扱います。これは、個々の電子がどのようなエネルギーを持ち、どの領域にいる可能性が高いかを示します。分子軌道は原子軌道の線形結合(LCAO: Linear Combination of Atomic Orbitals)として近似されることが多く、原子軌道同士の干渉(位相が合えば構成的、逆なら破壊的)によって形とエネルギーが決まります。
結合軌道と反結合軌道
- 結合(ボンディング)軌道:原子軌道の位相が同じ向きで重なり、電子密度が原子間に増加します。エネルギーは元の原子軌道より低く、分子を安定化します。
- 反結合(アンチボンディング)軌道:原子軌道の位相が逆で重なり、原子間にノード(波動関数がゼロの面)が現れます。エネルギーは高く、電子が入ると結合を弱めます。
- 非結合軌道:特定の原子に局在し、他の原子との重なりが小さい軌道。エネルギーは原子軌道に近い。
電子配置とエネルギー順序:HOMOとLUMO
分子では原子と同様に、軌道に電子が入る順序があります。主に以下の規則に従います:パウリの排他原理(同一軌道におけるスピンの制限)、ハウスの法則(低エネルギー軌道から順に占有)。
HOMO(Highest Occupied Molecular Orbital)は最もエネルギーの高い占有軌道、LUMO(Lowest Unoccupied Molecular Orbital)は最もエネルギーの低い空軌道です。HOMO–LUMOギャップは、化学反応性や光学特性を決める重要な指標です(ギャップが小さいほど反応性が高く、光吸収が長波長側にずれることが多い)。
代表的な例
- H2(水素分子):2つの1s原子軌道が同位相で重なってσ(結合)軌道を作り、低エネルギーになる。逆位相で重なるとσ*(反結合)軌道ができる。
- O2(酸素分子):π*(反結合)軌道に2つの未対電子があり、そのため酸素分子は常磁性を示す(パラ磁性)。これは分子軌道理論が古典的な結合モデルより優れている例です。
- CO(一酸化炭素):HOMOは炭素側に偏った孤立電子対的性質をもち、LUMOは反結合性質を示すため、金属錯体との配位化学で特有の挙動を示します。
分子軌道図の読み方(簡単な手順)
- 各原子の主要な原子軌道(s, p, d など)を並べる。
- エネルギーと対称性が近い軌道同士を組み合わせる(同じ対称性でしか混ざらない)。
- 干渉の種類(同位相=結合、逆位相=反結合)を決め、軌道エネルギーを並べる。
- 電子数に基づいて軌道に電子を入れ、HOMOとLUMOを確認する。
計算化学での扱い
実際の分子軌道は解析的に求めることが難しいため、コンピュータで近似解を求めます。代表的手法には
- ハートリー–フォック(HF)法:平均場近似で一電子軌道を求める。
- 密度汎関数理論(DFT):電子密度を主役にした実用的で広く使われる方法。多くの化学・材料研究で標準的。
- 基底関数(Basis set):原子軌道の組み合わせに用いる関数群。大きいほど精度は上がるが計算負荷も増える。
これらの計算により、軌道の形状(電子密度分布)、エネルギー、分子の安定性、電子遷移エネルギー(光吸収スペクトル)などが得られます。
応用例:反応性、光学、磁性
- 分子軌道を使えば、どの部分が求核剤(電子供与体)や求電子剤(電子受容体)として働くかを予測できる(HOMOは電子供与性、LUMOは電子受容性の指標)。
- 光吸収は電子がHOMOからLUMOへ遷移することで説明でき、吸収波長はHOMO–LUMOギャップに対応する。
- 磁性は未対電子の存在(例えばO2のπ*)で説明され、磁気的性質の予測にMO理論が使われる。
まとめ
分子軌道は、分子中の電子の波動的性質を表す基本概念であり、結合の有無や強さ、反応性、光学・磁気特性を理解・予測する強力な道具です。LCAOの考え方とエネルギー準位の整理(HOMO/LUMO)を押さえることで、分子の性質を直感的かつ定量的に扱えるようになります。詳しい解析はハートリー–フォックやDFTなどの計算手法を用いて行われます。