氷とは:定義・性質・摂氏0℃の凍結点と家庭での作り方
氷の定義・性質から摂氏0℃の凍結点、家庭での簡単な作り方まで図解でわかる入門ガイド。冷凍のコツや応用も紹介。
氷は、凍った水の一般的な名称です。アンモニアやメタン、牛乳など、他の液体も凍ると氷と呼ばれることがありますが、それらは単に「氷」ではなく、例えば「ミルクアイス」と呼ばれます。液体の水は、非常に冷たくなると固体の氷になります。凝固点は摂氏0度(華氏32度または273ケルビン)で、標準大気圧下での値です。
定義と基本的な性質
通常私たちが目にする氷は、常圧で安定な六方最密充填に近い結晶構造をもつ「氷Ih(アイ・エイチ)」と呼ばれる相です。氷は水と比べて体積が約9%増加するため密度が小さく、これが原因で氷は水面に浮きます。氷が溶けるときには融解潜熱(約334 kJ/kg)を周囲から奪うため、冷却や保存に広く利用されます。
その他の重要な性質:
- 透明度:純水をゆっくり凍らせると透明に近い氷ができるが、空気や不純物が閉じ込められると白く濁る。
- 熱伝導率:氷は固体としてある程度の熱を伝えるが、金属に比べれば低い。
- 力学特性:氷は脆く割れやすいが、温度や結晶方向によって強度が変わる。
- 多形性:高圧下では多くの異なる結晶相(氷II、氷IIIなど)が現れる。
凍結点と関連現象
標準条件での凍結点は0℃ですが、次のような影響を受けます。
- 溶質(塩など)の存在:溶質は凝固点を下げる(凝固点降下)。道路の融雪に塩を撒くのはこの原理。
- 圧力の影響:水は特殊な性質として圧力をかけると融点がわずかに低下する(氷の融点は圧力によって変化する)。
- 過冷却:純粋な水は核生成が起きない場合、0℃以下でも液体のまま過冷却状態になることがある。衝撃や種結晶で急に凍結することがある。
- 凍結の方向性:ゆっくり一方向から凍らせると気泡や不純物が追い出され、透明な氷が得られやすい。
家庭での作り方(作り方とコツ)
氷は家庭用の冷蔵庫や冷凍庫で簡単に作れます。以下は基本的な手順と工夫です。
基本的な作り方:
- 容器(製氷皿など)に水を入れる。
- 冷凍庫に入れ、凍るまで待つ(時間は水の量や冷凍庫の性能で異なる)。
- 凍ったら取り出して使用する。
凍る速度に関しては、文章にある通り銅などの金属製の容器に水を入れると早く氷になります。これは金属が熱伝導率が高いので、熱を効率よく冷凍庫へ伝えるためです。一方、プラスチック製の製氷皿は熱を伝えにくく、同じ量を凍らせるのに時間がかかります。
透明で美しい氷を作るコツ:
- 沸騰させて冷ました水を使うと溶存気体が減り、透明度が上がる。
- ゆっくり・一方向に凍らせる(保冷ボックス内に入れて上から凍らせるなど)と気泡や不純物が押し出されやすい。
- 密閉されたガラス容器で凍らせると破裂の危険があるので避ける。
- 金属製の型は速く凍るが、速い凍結は中心に気泡を閉じ込めることがあるため、用途に応じて選ぶ。
用途と安全性
氷は飲料の冷却、食品の保存、医療(外傷の冷却)、輸送(冷蔵輸送の補助)、冬季スポーツや景観(スケートリンク、雪氷彫刻)など多岐にわたる用途があります。自然界では氷河や海氷として気候や生態系にも重要な役割を果たします。
安全上の注意:
- 密閉容器での凍結は破裂の危険がある。
- 溶けた氷を再凍結すると品質が落ちる場合がある(食の安全に注意)。
- 冷凍庫から直接熱い物を入れると故障や凍結ムラの原因になる。
以上のように、日常で見かける氷には物理的・化学的な興味深い性質が多くあり、家庭でも簡単な工夫で用途に応じた氷が作れます。

バスケットの中の氷
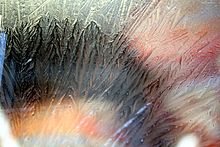
ガラスの上の氷の結晶
氷ができるまで
他の液体とは異なり、水は凍ると膨張して氷となり、氷は水よりも密度が低いため、水の上に氷が浮く。これは非常に珍しいことです。他のほとんどの液体は、冷えると密度が高くなりますが、水の氷は重要な例外です。液体の水は、氷になると約9%膨張し、より大きな空間を占めるようになります。これは、水の分子同士が接近するのではなく、実際には離れているからです。氷の結晶の分子は、液体の水よりも密度が低くなるように配置されています。配管の中の水が凍ると、水道管が破裂することがあります。ガラス瓶の中の水が凍ると、瓶が破裂することもあります。岩の割れ目で凍った水は、硬い岩を引き裂くほどに膨張します。これは、山をすり減らし、岩を土にする重要な地質学的風化プロセスです。
物質が冷やされると、分子の振動が弱まり、コンパクトにまとまります。ほとんどの物質は、凝固点と呼ばれる温度に達すると、分子が結晶性の固体を形成します。ただし、ガラスやタールのように、まったく結晶化せず、超硬い流体を形成して、固体のように見える物質もあります。ヘリウムだけは凍りません。その他の物質は十分に冷やせば凍りますが、食用油、不凍液、ガソリン、窒素などの流体は、一般の人が経験しない温度で凍ります。
塩水
塩水は純水よりも低い温度で凍ります。凍った氷には、元の塩水よりもはるかに少ない塩分しか含まれていない。この事実を利用して、海水淡水化が行われることもある。塩分を含んだ氷は、純水を凍らせたものほど強くありません。同様に、氷の上に塩を撒くと、寒すぎなければ氷は溶けます。塩は徐々に氷に食い込み、その温度では凍らない塩水を形成します。
氷の地理的位置
氷は浮くので、海のように大きな水域が凍っても、表面にしか氷ができません。ほとんどの湖は底まで凍ることはありません。北極海のような最も冷たい海でも、表面だけが凍り、下には液体の海が循環しています。このため、地球の海は熱を再分配することができ、地球の気候は極端な暑さや寒さが少なくなっています。もし氷が浮くのではなく沈むとしたら、海は底から氷で満たされて固くなり、上部の一部だけが融けることになる。固まった海では、熱が循環しません。しかし、氷が表面に浮かんでいるため、下の水は循環し続けることができ、表面の氷は露出したままで、温度が上がるとすぐに溶けてしまいます。陸地にある大きな氷は「氷河」と呼ばれている。世界の氷の大部分は南極大陸にある。
氷河期
気候変動は常に起こっています。非常に寒いときは氷河期と呼ばれます。氷河期には、地球の非常に広い範囲が氷、雪、氷河で覆われます。氷河期の原因は複雑であり、理解するのは難しい。現在、地球温暖化が地球の氷資源に影響を与えていますが、その原因も非常に複雑です。
ドライアイス
また、二酸化炭素を凍らせた「ドライアイス」もある。ドライアイスを通常の空気にさらすと、無臭・無色の炭酸ガスが発生する。このガスは非常に冷たく、空気と混ざると、空気中の水蒸気を冷やして霧にし、濃い白煙のように見えるのです。劇場では、霧や煙の演出によく使われる。

水の中に入れるとドライアイス
質問と回答
Q:氷とは何ですか?
A:氷は、凍った水の通称です。
Q: 他の液体も氷と呼べるのでしょうか?
A:はい、アンモニアやメタン、牛乳などの液体も凍ると氷になりますが、通常は「ミルクアイス」のような固有名称で呼ばれます。
Q:液体の水が固体の氷になるのはいつですか?
A:液体の水は非常に冷たく、その温度が0℃の氷点に達すると固体の氷になります。
Q: 家庭で氷はどのように作られるのですか?
A:氷は、家庭の冷蔵庫や冷凍庫で作るのが一般的です。冷凍庫に水を入れてしばらく放置しておくと、水が非常に冷たくなって固まり、氷ができます。
Q: 容器の材質によって、水が凍って氷になるまでの時間は変わるのでしょうか?
A: はい、銅(または他の金属)の容器に水を入れると、より早く氷になることができます。金属は熱伝導率が高いので、プラスチックの製氷皿に入れるよりも早く凍ることができます。
Q: 水の凝固点は何度ですか?
A:水の凝固点は0℃(32°F、273K)です。
Q: なぜ、ある液体は凍ったときに違う名前になるのですか?
A:「ミルクアイス」のように、凍ったときに違う名前になる液体がありますが、これは通常、凍ったときの性質に影響を与える他の成分を混ぜているためです。
百科事典を検索する